МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
БЕЛОРУССКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
КАФЕДРА ТРАВМАТОЛОГИИ И ОРТОПЕДИИ
Е.Р. Михнович
ОСТЕОХОНДРОПАТИИ
ОБЩАЯ ХАРАКТЕРИСТИКА ОСТЕОХОНДРОПАТИЙ
Остеохондропатии (osteochondropathii ; от греч. osteon – кость, chondros – хрящ, pathos – страдание; синонимы: остеохондрит, эпифизионекроз, остходролиз, асептический некроз костей) – это особая группа заболеваний костно-суставного аппарата с характерными клинико-рентгенологическими симптомами, в основе которых лежит асептический некроз губчатой костной ткани в местах повышенной механической нагрузки.
Как самостоятельное заболевание остеохондропатия впервые выделена в 1923 г. Аксхаузеном, затем эту патологию описал в 1927 г. Бергман. Однако еще раньше, в 1909 г., асептический некроз головки бедренной кости был описан Леггом, а в 1910 г. – Пертесом.
Этиология остеохондропатий до конца не выяснена. Можно выделить несколько факторов, которые играют определенную роль в развитии заболевания.
Врожденный фактор обусловлен особой врожденной или семейной предрасположенностью к остеохондропатиям. Известны случаи остеохондропатии бедра, наблюдавшиеся у членов одной семьи в течение нескольких поколений.
Эндокринные (гормональные) факторы связаны с нередким возникновением патологии у лиц, страдающих дисфункциями эндокринных желез , в том числе при акромегалии, миксидеме, гипотиреоидизме.
Обменные факторы проявляются в нарушении метаболизма при остеохондропатиях, в частности обмена витаминов и кальция. Опубликованы сообщения об асептическом некрозе костей, возникающем в связи с нарушениями метаболизма при длительном употреблении кортикостероидов, например, после трансплантации почек.
С давних пор отдельные авторы выдвигали инфекционные факторы как причину заболевания. Согласно их утверждениям, асептический некроз губчатой кости обусловлен эмболией кровеносных сосудов микробного происхождения, однако, с течением времени данное предположение не нашло убедительного подтверждения.
На сегодняшний день многие исследователи отдают предпочтение травматическим факторам. Здесь имеет значение как частая травма, так и чрезмерные нагрузки, в том числе и усиленные мышечные сокращения. Они приводят к прогрессирующему сдавлению, а затем и облитерации мелких сосудов губчатой кости, особенно в местах наибольшего давления.
Наряду с острой и хронической травмой, огромное внимание уделяется и нейротрофическим факторам, приводящим к сосудистым расстройствам. Согласно мнению М.В. Волкова (1985), изменения в скелете при остеохондропатиях являются следствием остеодистрофии ангионеврогенного характера.
Патологическая анатомия. В основе патологоанатомических изменений лежит асептический подхрящевой некроз тех участков губчатой костной ткани апофизов и эпифизов, которые находятся в условиях повышенной статической и функциональной нагрузки. В результате асептического остеонекроза постепенно развивается деструкция пораженной кости и суставного хряща с отделением секвестра и перестройкой внутренней костной структуры. При этом наступает изменение формы не только зоны поражения кости, но и развивается нарастающая деформация всего сустава с нарушением конгруэнтности суставных поверхностей.
Характерные признаки остеохондропатий
Наблюдаются исключительно в детском и юношеском возрасте (кроме рассекающего остеохондрита суставных поверхностей – болезни Кенига и остехондропатии полулунной кости кисти – болезни Кинбека).
Для остеохондропатий присуща определенная стадийность развития анатомических и рентгенологических признаков.
Характеризуются хроническим сравнительно доброкачественным клиническим течением и относительно благоприятным исходом.
Длительность заболевания зависит от локализации процесса и варьирует от 1 года до 5-6 лет (в отдельных наблюдениях – до 8 лет).
Остеохондропатии поражают эпифизы и апофизы трубчатых костей (длинных и коротких), некоторые короткие губчатые кости, апофизы и тела позвонков. Чаще всего процесс локализуется в костях нижних конечностей.
При локализации патологического процесса в области суставного эпифиза может возникать значительная деформация суставной поверхности и развиваться вторичный остеоартроз пораженного сустава.
Учитывая высокие репаративные возможности кости в период роста, основной метод лечения остеохондропатий – консервативный. При этом первостепенное значение имеет разгрузка пораженной конечности и проведение физиотерапевтических процедур.
Хирургическое лечение применяется не очень часто, в основном при развитии выраженной деформации в области поражения или наличии внутрисуставных тел, блокирующих движения в суставе (болезнь Пертеса, Кенига, Келлера II, Кинбека).
Стадии остеохондропатий
В течении остеохондропатий различают 5 стадий, которые отличаются друг от друга анатомической и рентгенологической картиной.
В I стадии (асептического некроза) вследствие сосудистых расстройств возникает субхондральный некроз губчатой кости и костного мозга, при этом суставной гиалиновый хрящ еще сохраняет жизнеспособность. В первые недели при рентгенологическом исследовании не обнаруживается четких признаков заболевания, однако, впоследствии (через 2-3 мес.) возникает незначительный остеопороз и смазанность костной структуры, происходит расширение суставной щели (за счет утолщения покровного хряща вследствие его дегенеративных изменений). В исходе данной стадии появляется слабое ограниченное уплотнение костного вещества в зоне некроза.
Стадия II (импрессионного перелома) наступает спустя несколько месяцев (обычно 3-4 мес., реже 6 мес.) от начала заболевания. Рентгенологически характерен так называемый «ложный склероз», обусловленный сдавлением, сплющиванием костных балок. Трабекулярная структура кости нарушается, уплотненная тень эпифиза уменьшается по высоте, ее контуры становятся волнистыми, фестончатыми. Суставная поверхность под действием нагрузки деформируется, а рентгеновская суставная щель расширяется. Длительность данной стадии около 3-5 мес. (иногда 6 мес.).
В стадии III (рассасывания или фрагментации) происходит медленное рассасывание некротизированной кости вследствие врастания тяжей молодой соединительной ткани. Пролиферация суставного и росткового хрящей в виде выступов хрящевой ткани приводит к разделению некротизированного участка кости на отдельные мелкие фрагменты. Рентгенологически определяются плотные секвестроподобные глыбки, разделенные участками просветления. Увеличивается деформация суставной поверхности, щель сустава остается расширенной. Продолжительность III стадии – 1-3 года.
В стадии IV (продуктивной или репарации) некротизированные костные фрагменты, а также соединительно-тканные и хрящевые тяжи постепенно замещаются новообразованным губчатым костным веществом. На рентгенограмме можно видеть рассасывание некротизированных костных балочек и образование новой кости с грубой структурой (иногда с развитием кистовидных полостей), в большей или меньшей степени приближающейся по форме к здоровому эпифизу. Длительность данной стадии от 6 мес. до 2 лет.
Следует подчеркнуть, что перечисленные стадии не строго отграничены друг от друга, а, напротив, тесно взаимосвязаны и взаимообусловлены. Поэтому процесс некроза сменяется процессами рассасывания и восстановления без резких и четких границ.
Стадия V (конечная) характеризуется законченным процессом перестройки костной структуры и восстановлением формы кости. Степень деформации восстановленного участка зависит от проведенных лечебных мероприятий и разгрузки сустава в период заболевания. При неполноценном, неправильном лечении либо сохраняющейся нагрузке на конечность возникает стойкая деформация поврежденной кости, развивается вторичный остеоартроз.
Классификация остеохондропатий
В зависимости от локализации патологического процесса выделяют 4 группы остеохондропатий:
I . Остеохондропатии эпифизарных концов трубчатых костей: 1) головки бедренной кости (болезнь Легга-Кальве-Пертеса); 2) головки II, реже III, плюсневой кости (болезнь Фрейберга-Келера II); 3) грудинного конца ключицы (болезнь Фридриха); 4) акромиального конца ключицы (болезнь Кливза); 5) головки плечевой кости (болезнь Хасса); 6) головки лучевой кости (болезнь Нильсона); 7) локтевого отростка (болезнь О’Коннора); 8) дистального эпифиза локтевой кости (болезнь Бернса); 9) шиловидного отростка локтевой кости (болезнь Мюллера); 10) головок пястных костей (болезнь Дитерикса); 11) проксимальных эпифизов фаланг пальцев кисти (болезнь Тиманна).
II . Остеохондропатии коротких губчатых и сесамовидных костей: 1) тела позвонка (болезнь Кальве, или плоский позвонок); 2) надколенника (болезнь Синдинга-Ларсена); 3) ладьевидной кости стопы (болезнь Келера I); 4) сесамовидной кости I плюснефалангового сустава (болезнь Ренандера-Мюллера); 5) полулунной кости (болезнь Кинбека); 6) ладьевидной кости кисти (болезнь Прайзера); 7) большой многоугольной кости (болезнь Хармса); 8) крючковидной кости (болезнь Фогеля); 9) гороховидной кости (болезнь Шмира).
III . Остеохондропатии апофизов (апофизиты): 1) апофизов тел позвонков (болезнь Шойерманна-Мау, или юношеский кифоз); 2) гребней подвздошных костей (болезнь Муше-Сорреля-Стефани); 3) лонно-седалищного сочленения (болезнь Ван Нека); 4) бугристости большеберцовой кости (болезнь Осгуда-Шлаттера); 5) бугра пяточной кости (болезнь Хаглунда-Шинца); 6) бугристости V плюсневой кости (болезнь Изелина).
Частичные клиновидные остеохондропатии суставных поверхностей (osteochondritis dissecans , рассекающий остеохондроз): 1) головки и дистального эпифиза бедренной кости (болезнь Кенига); 2) головки плеча; 3) дистального эпифиза плечевой кости (болезнь Паннера); 4) тела таранной кости (болезнь Диаза).
ХАРАКТЕРИСТИКА НАИБОЛЕЕ РАСПРОСТРАНЕННЫХ ОСТЕОХОНДРОПАТИЙ
Остеохондропатия головки бедренной кости
(болезнь Легга-Кальве-Пертеса)
(Osteochondropathia caput femoris )
Остеохондропатия головки бедренной кости впервые была описана в 1909-1910 гг. независимо друг от друга Вальденстромом в Швеции, Леггом в США, Кальве во Франции и Пертесом в Германии.
Патология относится к числу распространенных: среди ортопедических больных встречается в 0,17-1,9% случаев. Среди заболеваний тазобедренного сустава в детском возрасте остеохондропатия головки бедра составляет до 25,3%.
Болеют дети преимущественно в возрасте от 4 до 12 лет, но известны случаи заболевания в более раннем и более позднем возрасте. Мальчики страдают чаще девочек (в 4-5 раз). Левый тазобедренный сустав поражается несколько чаще, чем правый. Двусторонняя локализация процесса наблюдается в 7-10% случаев. Для остеохондропатии головки бедра характерно длительное течение (в среднем, 2-4 года, а иногда до 5-6 лет).
Заболевание протекает по типу первичного асептического некроза и возникает вследствие сосудистых расстройств в субхондрально расположенном губчатом веществе головки бедренной кости. В качестве этиологических факторов рассматриваются микротравма, перегрузка на фоне конституциональной предрасположенности, нарушение нормального процесса окостенения эпифиза головки бедренной кости в возрасте 3-8 лет (Пертес-возраст), связанное с субкритическим его кровоснабжением вследствие врожденного недоразвития локальной сосудистой сети. Не исключается наследственный фактор в развитии заболевания, а также влияние очагов хронической инфекции. В последние десятилетия высказывается мнение о диспластической природе патологии, согласно которому причиной сосудистых нарушений и некроза головки является патологическая ориентация компонентов тазобедренного сустава.
На сегодняшний день с помощью современных методов исследования (радиоизотопного, капилляроскопического, термометрического и др.) установлено, что нарушения артериального и венозного кровообращения имеются на всей нижней конечности, а не только в области тазобедренного сустава. Кроме того, согласно современному представлению о патогенезе болезни Пертеса, имеет место поражение не только головки бедра, но и всех элементов тазобедренного сустава – вертлужной впадины с суставным хрящом, эпифизарного хряща, шейки бедра вместе со всем метафизом проксимального отдела бедренной кости, капсулы сустава. Поэтому, по мнению многих авторов, есть все основания называть болезнь Пертеса остеохондропатией тазобедренного сустава.
Клиника. Остеохондропатия головки бедренной кости развивается медленно, вначале незаметно, что затрудняет диагностику заболевания на ранних стадиях развития процесса. Первые симптомы болезни – боль и щадящая хромота. Боль часто носит приступообразный характер, сменяясь светлыми промежутками. При этом в начальной стадии у 75% детей болевые ощущения локализуются не только в тазобедренном суставе, но иррадиируют в область коленного сустава (так называемые «отраженные» боли). Появляется утомляемость при ходьбе, щадящая хромота. Со временем нарастает гипотрофия мышц бедра и ягодичной области, наступает ограничение движений, особенно отведения и внутренней ротации . Возникает укорочение конечности, которое вначале является кажущимся (вследствие сгибательно-приводящей контрактуры в тазобедренном суставе). С прогрессированием процесса и уплощением головки бедренной кости, а также в связи с развивающимся ее подвывихом появляется истинное укорочение бедра на 2-3 см. Большой вертел на стороне поражения смещается выше линии Розера-Нелатона. Иногда выявляется положительный симптом Тренделенбурга. При неправильном лечении патологический процесс заканчивается деформацией головки и развитием остеоартроза с упорным болевым синдромом и нарушением функции тазобедренного сустава.
Рентгенологическое обследование помогает в постановке диагноза. Для сравнительного анализа производят рентгеновские снимки обоих тазобедренных суставов, а также рентгенограмму в положении Лауэнштейна. Наиболее полную информацию о локализации и распространенности патологических изменений в головке бедра дает компьютерная и ядерно-магнитно-резонансная томография тазобедренных суставов. В ранней диагностике заболевания высокоэффективно радиоизотопное исследование (сцинтиграфия).
Изменения на рентгенограммах зависят от стадии процесса.
В I стадии (асептического некроза губчатой кости эпифиза и костного мозга) изменения отсутствуют либо незначительные: в виде остеопороза костей, образующих тазобедренный сустав, извилистости и неравномерности хрящевой эпифизарной пластинки, неоднородности и пятнистости шейки бедра, некоторого расширения щели сустава.
Во II стадии (импрессионного перелома) головка бедренной кости утрачивает характерную трабекулярную структуру, шейка бедра становится более остеопоротичной. Суставная щель отчетливо расширяется по сравнению со здоровым тазобедренным суставом. Эпифиз головки уплотняется, склерозируется и деформируется (вследствие сохраняющейся нагрузки).
В III стадии (фрагментации эпифиза) суставная щель по-прежнему расширена, головка сплющена и как бы разделена на отдельные глыбки или неправильной формы мелкоочаговые фрагменты. Обычно определяется от 2 до 5 таких фрагментов, а иногда и больше. Вертлужная впадина уплощается.
В IV стадии (репарации) определяется формирование новых костных балочек, эпифиз полностью замещается новообразованной костью с участками просветления в центре.
В V стадии (конечной) завершается структурная перестройка и восстановление формы головки и шейки бедра. Суставная щель суживается и приближается по своей величине к нормальной. Если лечение было правильным, форма восстановленной головки незначительно отличается от сферической; в противном случае формируется грибовидная головка с укороченной расширенной шейкой. При этом вертлужная впадина не полностью покрывает увеличенную деформированную головку, что впоследствии приводит к развитию вторичного коксартроза.
Лечение при болезни Пертеса должно начинаться как можно раньше, чтобы предотвратить развитие морфологических изменений и нарушение функции сустава.
В основе консервативного лечения лежит ранняя и длительная разгрузка конечности , что позволяет сохранить форму головки бедренной кости. Назначают постельный режим с накожным или скелетным вытяжением за больную ногу, ходьбу на костылях без нагрузки на пораженную конечность, применяют специальную петлю для подвешивания ноги, согнутой в коленном суставе, за нижнюю треть голени. Используют отводящие шины с шарнирами на уровне суставов или ортопедические аппараты, обеспечивающие значительное уменьшение избыточного давления на головку бедренной кости. Разгрузка не должна исключать движения в суставе, поэтому для укрепления мышц тазобедренного сустава и всей нижней конечности назначают лечебную физкультуру, плавание в бассейне, массаж.
С целью улучшения репаративных процессов назначают медикаментозное лечение и физиотерапевтические процедуры. В зависимости от стадии заболевания применяют препараты, улучшающие кровообращение (трентал, никотиновая кислота, никошпан) и стимулирующие репаративные процессы (неробол, АТФ, витамины группы В). Используют электропроцедуры (УВЧ, электрофорез, ультразвук, диатермию), способствующие рассасыванию некротической ткани и процессу костеобразования, а также тепловые процедуры (парафин, озокерит, грязелечение, тепловые ванны), улучшающие кровоток в зоне поражения. Наилучшие условия для консервативного лечения созданы в специализированных санаториях. Средний срок консервативной терапии – 2-3 года.
Виды оперативных вмешательств. В начальных стадиях заболевания без признаков выраженной деформации для ускорения репаративных процессов осуществляют введение костного аутотрансплантата в эпифиз головки бедренной кости. Широкое распространение в последние десятилетия приобретают и микрохирургические операции по удалению некротизированного участка эпифиза с его полным замещением трансплантатом на сосудистой питающей ножке.
При прогрессировании патологических изменений в головке и шейке бедра и нарушении пространственных взаимоотношений компонентов тазобедренного сустава применяют различные внесуставные реконструктивные вмешательства , позволяющие не только вывести из-под нагрузки пораженный участок эпифиза, но и произвести восстановление нарушенных взаимоотношений в тазобедренном суставе. Чаще всего используют межвертельную деторсионно-варизирующую остеотомию бедра, позволяющую уменьшить шеечно-диафизарный угол и корригировать избыточную антеторсию проксимального отдела бедра. В случаях формирования деформации с уменьшенным шеечно-диафизарным углом, что сопровождается укорочением конечности, применяют деторсионно-вальгизирующую остеотомию бедра. В результате данных вмешательств не только улучшается центрация головки бедренной кости в вертлужной впадине, но и происходит биологическое раздражение тканей, приводящее к реактивной гиперемии и активно способствующее быстрейшему восстановлению структуры головки.
Исключительно важным и успешным этапом поиска новых оптимальных оперативных вмешательств при болезни Пертеса является ротационная остеотомия бедренной кости, разработанная в 1978 г. японским ортопедом Sugioka (передняя ротационная чрезвертельная) и в 1980 г. белорусским ортопедом А.М. Соколовским (задняя ротационная межвертельная, или операция взаимозамещения). При операции взаимозамещения проксимальный фрагмент, включающий головку и шейку бедренной кости, поворачивается на 45-90° кзади. Данное вмешательство позволяет вывести пораженный верхний полюс эпифиза бедра из-под нагрузки и полностью заменить его сохранившимся в целости неповрежденным сегментом.
Корригирующие остеотомии бедренной кости при болезни Пертеса не всегда приводят к восстановлению правильных соотношений в тазобедренном суставе. Поэтому для коррекции тазового компонента деформации используют надвертлужную остеотомию таза по Солтеру, позволяющую увеличить покрытие головки бедра.
Хирургические вмешательства при остеохондропатии головки бедра позволяют сократить сроки лечения заболевания в 1,5 раза и способствуют снижению инвалидизации данной категории больных.
Остеохондропатия бугристости большеберцовой кости
(болезнь Осгуда-Шлаттера)
(Osteochondropathia tuberositas tibiae )
Заболевание впервые описано Осгудом (США) и Шлаттером (Швейцария) в 1903 г. В научной литературе известно как асептический некроз бугристости большеберцовой кости, апофизит большеберцовой кости, болезнь Лауба, болезнь Ланелонга-Осгуда-Шлаттера.
Чаще болеют мальчики в возрасте от 13 до 15-18 лет. Нередко встречается двусторонняя локализация процесса. В основе заболевания лежит нарушение процессов окостенения бугристости большеберцовой кости. Остеохондропатия часто развивается без видимой причины, однако, иногда удается установить связь с повторной травмой или повышенной функцией четырехглавой мышцы бедра (например, при занятиях спортом или балетом).
Клиника. Отмечается припухлость и локальная боль в области бугристости большеберцовой кости, усиливающаяся при пальпации. Зачастую определяется выраженное увеличение апофиза большеберцовой кости (в 2 раза и более). Движения в коленном суставе болезненны, особенно после физической нагрузки. Крайняя степень сгибания конечности в коленном суставе сопровождается выраженными болевыми ощущениями, нередко сохраняющимися и в состоянии покоя.
При рентгенологической диагностике болезни Осгуд-Шлаттера необходимо иметь в виду множество вариантов нормальной оссификации апофиза большеберцовой кости. Чаще всего апофиз окостеневает в виде хоботообразного отростка в возрасте 10-13 лет, но встречаются варианты с добавочными мелкими ядрами окостенения. Слияние апофиза с метафизом происходит в 16-18 лет.
При остеохондропатии определяются неправильные нечеткие контуры бугристости и ее фрагментация на несколько секвестроподобных фрагментов.
При диагностике всегда следует учитывать несоответствие между значительным выбуханием бугристости при клиническом исследовании и почти нормальными размерами апофиза на рентгенограмме. Предпочтение необходимо отдавать клиническим данным.
Заболевание продолжается около года и заканчивается восстановлением структуры апофиза. Функция коленного сустава, как правило, не страдает.
Лечение, прежде всего, требует исключения всяких перегрузок и создания относительного покоя, вплоть до кратковременной иммобилизации, и основано на физиотерапевтических методах (магнитотерапия, электрофорез с кальцием и новокаином, бальнеотерапия и грязелечение). Оперативное лечение, как правило, не применяется, за исключением единичных случаев отрыва бугристости при повышенной физической нагрузке. Отшнуровавшиеся в результате перенесенного заболевания болезненные костно-хрящевые тела также могут быть удалены хирургическим путем.
Остеохондропатия апофизов тел позвонков
(болезнь Шойерманна-Мау)
(Osteochondropathia apophisis corpus vertebrae )
Остеохондропатия апофизов тел позвонков (асептический некроз апофизов тел позвонков, или болезнь Шойерманна-May, болезнь Шморля, остеохондропатический кифоз, юношеский кифоз) встречается чаще у юношей в период роста организма в возрасте 11-18 лет. Заболевание впервые было описано в 1921 г. ортопедом Шойерманном, патологоанатомом Шморлем и хирургом May (1924). Относится к довольно распространенному заболеванию детского возраста, составляя от 0,42 до 3,7%.
Основой остеохондропатии позвоночника считают врожденную неполноценность дисков и недостаточную прочность замыкательных пластинок тел позвонков. Отмечают влияние гормональных факторов (заболевание нередко сочетается с эндокринными расстройствами), а также наследственную предрасположенность (возможно наследование по аутосомно-доминантному типу). В прогрессировании деформации немаловажную роль играет фактор нагрузки (неправильный режим, долгое сидение в согнутом положении, тяжелая физическая работа, перенос грузов на спине).
Как показывают рентгенологические исследования нормального позвоночника, в возрасте 10-12 лет в межпозвонковых хрящевых дисках появляются добавочные апофизарные точки окостенения тела позвонка, имеющие треугольную форму на рентгенограмме в боковой проекции (рис. 6). Процесс их костного слияния начинается в возрасте 14-15 лет, а в 18-20 лет заканчивается. В результате тело позвонка из двояковыпуклой формы, характерной для детского возраста, превращается в двояковогнутую, которая присуща взрослому человеку.
Нарушение энхондральной оссификации в области зон роста тел позвонков (апофизарных зон) при болезни Шойерманна-May и приводит к возникновению их клиновидной деформации и формированию кифоза. Чаще поражаются 3-4 средних или нижнегрудных позвонка, локализация процесса в поясничном отделе позвоночного столба довольно редкая. Наиболее типично вовлечение в патологический процесс VII, VIII, IX и X грудных позвонков.
Клиника заболевания отличается медленным развитием и в течение ряда лет проходит 3 стадии.
I стадия продолжается до появления оссификации апофизов тел позвонков и характеризуется несколько увеличенным грудным кифозом.
Во время II стадии (с появлением окостенения апофизов) формируются все типичные признаки заболевания. Появляется боль в спине, особенно при длительной ходьбе и сидении, возникает быстрая утомляемость и слабость мышц спины. Происходит увеличение патологического кифоза с вершиной, расположенной на уровне Th8-L1. Его образование сопровождается усилением лордоза в шейном и поясничном отделах, одновременно может сформироваться и сколиоз. Деформация приобретает фиксированный характер. Присоединение корешкового синдрома дискогенного происхождения приводит к еще большему ограничению подвижности позвоночника.
В III стадии процесса, соответствующей полному слиянию апофизов с телами позвонков, кифоз и клиновидная деформация тел позвонков несколько уменьшаются. Однако фиксированный кифоз и увеличенный поясничный лордоз остаются в течение всей жизни. Со временем развиваются явления остеохондроза позвоночника с нарастающим болевым синдромом.
Рентгенологически изменения, характерные для остеохондропатии, определяются во II стадии заболевания. Выявляются зазубренность апофизов, клиновидная деформация тел позвонков с увеличением их переднезаднего размера, сужение межпозвонковых дисков, нарушение целостности замыкательных костных пластинок позвонков с образованием грыж Шморля. Формируется патологический кифоз грудного отдела позвоночника.
Лечение. Рекомендуют общеукрепляющее лечение, витаминотерапию, рациональный режим труда и отдыха (спать на жестком), выработку правильной осанки, разгрузку позвоночника. С целью укрепления мышечного корсета назначают лечебную гимнастику, плавание в бассейне, массаж мышц спины. Некоторые авторы рекомендуют ношение корсета с пелотом на вершине деформации в положении разгибания позвоночного столба. При рано начатом лечении удается приостановить развитие процесса и образование выраженной деформации. В единичных случаях при выраженном кифозе с неврологическими проявлениями показано оперативное лечение.
Остеохондропатия тела позвонка
(болезнь Кальве, плоский позвонок)
(Osteochondropathia corpus vertebrae )
Заболевание впервые описано Кальве в 1925 г. Встречается редко, в основном у мальчиков в возрасте 7-14 лет. В основе патологии лежит асептический некроз губчатого вещества тела позвонка. Длительность заболевания от 2 до 5-6 лет.
Клиника. Проявляется чувством усталости в спине, болью в позвоночнике, болезненностью при надавливании на выступающий остистый отросток пораженного позвонка. Наклон кпереди и разгибание позвоночника могут быть ограниченными, возможны корешковые симптомы. У большинства детей общее самочувствие хорошее, температура тела нормальная, однако, в отдельных случаях заболевание начинается с подъема температуры до 39,0°С, повышения СОЭ и эозинофилии.
На рентгенограмме в профильной проекции пораженный позвонок уплотнен, равномерно сплющен и расширен в переднезаднем направлении (платибрахиспондилия). Тело позвонка приобретает вид узкой полоски, передний край его выступает кпереди, межпозвонковые щели расширены.
Лечение. Основа лечения – разгрузка позвоночного столба (постельный режим на спине на жесткой постели или в гипсовой кроватке с реклинирующим валиком под пораженным позвонком) и лечебная гимнастика. Лежа проводят массаж, общую и лечебную гимнастику, направленную на реклинацию уплощенного позвонка и укрепление мышц спины (создание мышечного корсета). В стадии восстановления рекомендуют ношение съемного ортопедического корсета, разгружающего позвоночный столб. Отдельные авторы считают целесообразным выполнение заднего спондилодеза с целью стабилизации позвоночника и быстрейшей вертикализации (подъема в вертикальное положение) пациента.
Остеохондропатия головок II - III плюсневых костей
(болезнь Фрейберга-Келера II )
(Osteochondropathia metatarsalis)
Остеохондропатия головки II плюсневой кости впервые описана Фрейбергом в 1914 г. и Келером в 1920 г. Заболевание встречается преимущественно у девочек в возрасте 10-20 лет. Локализуется в эпифизе головки II, реже III, плюсневой кости. В единичных случаях возможно вовлечение в патологический процесс IV и V, а также одновременное поражение II и III плюсневых костей.
Причинами патологии считают хроническую микротравму, статические перегрузки переднего отдела стопы при плоскостопии или вследствие ношения обуви на высоком каблуке. Заболевание чаще возникает справа. Длительность течения процесса 2-2,5 года, развитие болезни постепенное.
Клиника . Отмечается боль в области головки соответствующей плюсневой кости, усиливающаяся при ходьбе и длительном стоянии. На тыле стопы в области поражения появляется отек без признаков воспаления. Активные и пассивные движения в плюснефаланговом суставе ограничены, может возникнуть укорочение соответствующего пальца. Больные ходят с опорой на пятку, разгружая передний отдел стопы. Боль сохраняется довольно продолжительное время, затем постепенно стихает.
В классическом варианте заболевание проходит 5 стадий, как и при болезни Легга-Кальве-Пертеса.
Рентгенологические изменения в I стадии могут отсутствовать. Во II стадии (импрессионного перелома) головка плюсневой кости теряет свою правильную шаровидную или овоидную форму и уплощается, длина ее уменьшается в 2-3 раза, приводя к укорочению соответствующего пальца. В III стадии происходит выраженное расширение суставной щели, секвестрация головки с образованием нескольких фрагментов, а в IV (репарации) – резорбция некротизированной кости с ремодуляцией головки, приобретающей блюдцеобразную форму. V стадия характеризуется развитием вторичного остеоартроза пораженного сустава.
Заболевание не всегда повторяет классическую стадийность остеохондропатий, поэтому отдельные авторы выделяют лишь 3 основные стадии: склероза, фрагментации и деформации головки с частичным восстановлением костной структуры губчатого вещества кости.
Лечение консервативное. При острых болях и выраженном отеке стопу фиксируют гипсовой лонгетой. После исчезновения острых явлений назначают ортопедическую обувь или стельки-супинаторы, обеспечивающие разгрузку соответствующей головки плюсневой кости. Одновременно проводят электропроцедуры, грязелечение, аппликации парафина и озокерита.
При развитии в области плюснефалангового сустава выраженной деформации с краевыми остеофитами и сильным болевым синдромом выполняют субтотальную моделирующую резекцию измененной головки. Известны операции эндопротезирования удаленной головки плюсневой кости, однако, они не получили широкого практического применения.
Остеохондропатия ладьевидной кости стопы (болезнь Келера I )
(Osteochondropathia os naviculare )
Асептический некроз ладьевидной кости стопы встречается преимущественно у мальчиков в возрасте 3-6 лет, но может наблюдаться и в более позднем возрасте (до 12 лет). Впервые описан Келером и Генишем в 1908 г.
В качестве этиологических факторов называют травму, а также нарушение развития ладьевидной кости, обусловленное рахитом. Длительность заболевания – 1-2 года.
Клиника. Возникают боли, усиливающиеся при ходьбе, и отек тыльной поверхности стопы по ее медиальному краю. Пальпация в проекции ладьевидной кости вызывает выраженную болезненность. С прогрессированием процесса болевой синдром усиливается, при ходьбе опора идет на наружный край стопы, появляется хромота.
На рентгенограмме в начальной стадии выявляется легкий остеопороз, затем уплотнение костной структуры ядра окостенения ладьевидной кости (ядер окостенения может быть несколько). Появляется сплющивание и фрагментация ладьевидной кости, ее деформация в виде чечевицы или полумесяца. Прилежащие суставные щели расширяются.
Лечение консервативное: разгрузка и иммобилизация конечности гипсовой повязкой с моделированием продольного свода стопы до 1-1,5 мес., затем ограничение статических нагрузок, тепловые процедуры, массаж, электрофорез иодида калия и новокаина, ношение стелек-супинаторов или ортопедической обуви.
Частичные клиновидные остеохондропатии
суставных поверхностей (рассекающий остеохондроз,
osteochondritis dissecans ) (болезнь Кенига)
Рассекающие остеохондриты суставных поверхностей – это остеохондропатии с единым этиопатогенезом и различной анатомической локализацией. В основе заболевания лежит нарушение кровообращения в ограниченном участке эпифиза. В результате формируется краевой асептический некроз небольшого участка субхондрально расположенной губчатой кости, форма которого напоминает чечевицу, двояковыпуклую или плосковыпуклую линзу. В дальнейшем происходит полное отделение этого костного фрагмента, покрытого гиалиновым хрящом, в полость сустава и превращение его в «суставную мышь», блокирующую движения в суставе.
Заболевание впервые описано Монрое в 1726 г. и Кенигом в 1888 г. По данным Центрального НИИ травматологии и ортопедии, среди ортопедических больных составляет 0,8%, а у пациентов с заболеваниями коленного сустава – 2%. Встречается в возрасте 11-60 лет, однако, преимущественно наблюдается у молодых мужчин от 20 до 40 лет.
В 90-93% случаев заболевание поражает коленный сустав, в основном внутренний мыщелок бедра. Патологический очаг может также локализоваться в области головки бедра, головки плеча, дистального эпифиза плечевой кости – болезнь Паннера (1929), головки луча, локтевого отростка, тела таранной кости – болезнь Диаза (1928), тела позвонка, головки I плюсневой кости.
Этиология заболевания окончательно не выяснена. Наибольшее признание получила сосудистая теория, согласно которой аваскулярный некроз возникает вследствие рефлекторного спазма или эмболии конечных сосудов, питающих ограниченный участок эпифиза. Высказываются предположения о влиянии
диспластических, нервно-сосудистых, травматических и эндокринных факторов.
Клиника . В развитии патологического процесса выделяют 3 стадии (З.С. Миронова, И.А. Баднин, 1976).
Клиническая картина в I стадии заболевания бедна симптомами. Боль в коленном суставе разной интенсивности, носит неопределенный перемежающийся характер, возникают явления умеренного синовита с небольшой припухлостью сустава.
С прогрессированием заболевания (II стадия ) боль принимает более постоянный характер, усиливается при ходьбе. Больные испытывают чувство тугоподвижности в суставе, снижается опорная функция конечности, появляется хромота.
После отделения в полость сустава некротизировавшегося костно-хрящевого фрагмента (III стадия ), иногда удается прощупать свободно перемещающееся внутрисуставное тело. Величина его может быть от крупной чечевицы до фасоли средних размеров, при ущемлении «суставной мыши» между суставными поверхностями возникает резкая боль и внезапное ограничение движений – блокада сустава. Со временем развивается гипотрофия четырехглавой мышцы бедра и возникают явления остеоартроза.
Рентгенологически в I стадии в субхондральной зоне выпуклой суставной поверхности мыщелка бедра выявляется ограниченный участок уплотнения кости. Обычно он двояковыпуклый, достигает размеров 1,0×1,5 см и ограничен узким ободком просветления. Затем (во II стадии ) происходит отграничение уплотненного костно-хрящевого фрагмента от материнского ложа: расширяется зона просветления вокруг него, фрагмент начинает выступать в полость сустава (рис. 10). В III стадии определяется ниша в области суставной поверхности мыщелка бедренной кости, а внутрисуставное тело обнаруживается в любой части коленного сустава (обычно, в одном из заворотов, а при блокаде сустава – между суставными поверхностями).
Аналогичные изменения могут наблюдаться и при частичных остеохондропатиях суставных поверхностей головки бедренной, плечевой и лучевой кости, головчатого возвышения плеча, локтевого отростка, блока таранной кости и некоторых других костей.
Лечение рассекающего остеохондрита зависит от стадии заболевания.
При I и II стадии показано консервативное лечение, включающее ограничение нагрузки с полным исключением прыжков и бега, иммобилизацию пораженной конечности лонгетой, физиотерапевтические процедуры (фонофорез хондроксида или гидрокортизона, электрофорез хлорида кальция, парафино-озокеритовые аппликации), применение хондропротекторов (мукосата, структума).
Оперативное лечение показано в III стадии заболевания (при наличии свободного костно-хрящевого фрагмента, блокирующего сустав и поддерживающего явления хронического синовита), а также является методом выбора при II стадии патологических изменений.
Хирургическое вмешательство выполняют с использованием артроскопической техники. При артроскопии не только уточняют диагноз, но одновременно удаляют некротически измененный участок суставной поверхности, распознаваемый по пожелтевшему, потерявшему блеск, размягченному гиалиновому хрящу. Костное ложе обрабатывают, края его заглаживают, при необходимости выполняют туннелизацию.
Если указанный фрагмент отделился и располагается в полости сустава в виде свободного тела, его находят и также удаляют. При больших размерах «суставной мыши», специальным инструментом фиксируют фрагмент в наиболее доступном отделе сустава, а удаление проводят через дополнительный разрез. В последние годы при значительных дефектах суставной поверхности мыщелков бедра, возникающих при болезни Кенига, выполняют замещение дефектов костно-хрящевыми ауто- или аллотрансплантатами.
Остеохондропатия полулунной кости кисти (болезнь Кинбека)
(Osteochondropathia ossis scaphoidei manus )
Заболевание впервые описано австрийским рентгенологом Кинбеком (1910). В основе патологии лежит субхондральный некроз полулунной кости запястья. Наблюдается преимущественно у лиц мужского пола в возрасте от 17 до 40 лет, подверженных частым повторным травмам кисти. Играет значение и постоянное перенапряжение кисти в процессе интенсивного ручного труда у слесарей, токарей, плотников, столяров. Процесс чаще локализуется на правой руке.
Клиника. Отмечается локальная боль и припухлость в области полулунной кости. При движениях и пальпации болевые ощущения усиливаются, особенно при разгибании кисти, сжатой в кулак. Постепенно нарастает ограничение подвижности в лучезапястном суставе, больше страдает тыльная флексия кисти. Сила сжатия пальцев в кулак значительно снижена, развивается гипотрофия мышц предплечья. Исход заболевания – остеоартроз суставов запястья, обусловленный возникновением в них подвывихов из-за уменьшения в объеме полулунной кости.
При рентгенологическом исследовании в ранней стадии заболевания отмечается смазанная картина структурного рисунка полулунной кости. Со временем тень ее становится более интенсивной по сравнению с соседними костями запястья, размеры уменьшаются, появляется неровность контуров, могут возникать кистозные изменения. В дальнейшем развивается фрагментация, сплющивание и прогрессирующая деформация полулунной кости, которая часто приобретает треугольную форму. Смежные суставные щели при этом расширяются. В редких случаях происходит уменьшение размеров полулунной кости с явлениями повышенного склероза костной ткани, напоминающего мраморную болезнь. В позднем периоде заболевания рентгенологически определяются явления остеоартроза.
Лечение. В начальных стадиях применяют консервативное лечение: фиксацию лучезапястного сустава гипсовой лонгетой в положении легкой тыльной флексии, тепловые процедуры, ультразвук, магнито- и лазеротерапию. При ранней диагностике и длительном лечении консервативная терапия дает определенный положительный эффект.
Существует более 20 способов оперативного лечения болезни Кинбека. В начальных стадиях заболевания для уменьшения сплющивания полулунной кости применяют метод лигаментотензии (растяжения) в аппарате Илизарова. При развитии выраженной деформации достаточно высокой эффективностью в плане улучшения функции кистевого сустава обладают частичные артродезы, включающие полулунную кость: полулунно-лучевой, запястный, полулунно-трехгранный артродез. При субтотальном и тотальном поражении прибегают к полному удалению некротизированной полулунной кости. Выполняют остеотомию головчатой кости и транспонируют ее головку на место полулунной по Гранеру (1966). Образовавшийся диастаз между фрагментами головчатой кости заполняют костным аутотрансплантатом.
Разработаны способы полного замещения полулунной кости силиконовыми эндопротезами ЦИТО и Свенсона, но они не получили широкого распространения.
Остеохондропатия бугра пяточной кости
(болезнь Хаглунда-Шинца)
(Osteochondropathia tuber calcanei )
Остеохондропатия апофиза пяточной кости описана Хаглундом в 1907 г. и Шинцем в 1922 г. как асептический некроз апофиза пяточной кости. Чаще встречается у девочек в возрасте 12-16 лет. Причина возникновения – частая травма пяток и перенапряжение ахиллова сухожилия и сухожилий подошвенных мышц при занятиях спортом.
Клиника. Заболевание начинается с острых или постепенно нарастающих болей в области бугра пяточной кости, возникающих после нагрузки. При пальпации или разгибании стопы болевой синдром усиливается. Над пяточным бугром, у места прикрепления ахиллова сухожилия, отмечается припухлость. Пациенты ходят с опорой на передний отдел стопы; бег, прыжки, занятия спортом становятся невозможными.
На рентгенограммах , особенно в боковой проекции, определяется уплотнение апофиза, расширение щели между апофизом и пяточной костью. Трудности рентгенологической диагностики связаны с тем, что в норме апофиз пяточной кости у детей имеет до 4-х ядер окостенения, среднее из которых, как правило, уплотнено, а смежные поверхности пяточной кости и апофиза зазубрены.
Наиболее характерным рентгенологическим признаком остеохондропатии является пятнистая структура уплотненного ядра окостенения. В дальнейшем наступает фрагментация апофиза, а затем и его перестройка – формируется новое губчатое вещество кости.
Лечение консервативное. Ограничивают физическую нагрузку, на время лечения прекращают занятия спортом. Применяют теплые ванночки и физиотерапевтическое лечение: электрофорез новокаина, ультразвук, диатермию. При сильном болевом синдроме назначают постельный режим, накладывают гипсовую повязку с моделированием сводов стопы. После ликвидации болей разрешают нагрузку на конечность в обуви с широким устойчивым каблуком. Для ослабления нагрузки на пяточную кость рекомендуют ношение ортопедических стелек-супинаторов с выкладкой продольного и поперечного сводов. В отдельных случаях применяют туннелизацию бугра пяточной кости по Беку.





















информация для прочтения
Остеохондропатия — некроз (омертвение) участка кости вследствие различных причин. Страдает также и прилежащая к кости хрящевая ткань. Болезнь протекает хронически, постепенно вызывая деформацию костей и суставов, с возрастом присоединяется артроз, ограничение подвижности (контрактура). Чаще всего болеют дети и подростки в возрасте 5-14 лет, но остеохондропатия у взрослых также имеет место. В структуре ортопедической заболеваемости она составляет 2,5-3% от общего числа обращений.
Нарушение поступления крови по артериям, идущим к эпифизу кости, приводит к развитию и остеохондропатии
Причиной остеохондропатии является нарушение кровообращения на участке кости вблизи сустава (эпифиза), приводящее к его омертвению и связанным с ним осложнениям — деформации, переломам. К расстройству кровоснабжения могут привести следующие факторы:
- Травмы: ушибы, гематомы, повреждения мягких тканей, кости, хряща.
- Гормональные и обменные нарушения, в основном в пубертатный (подростковый) период, недостаток солей фосфора и кальция.
- Недостаток белка в диете (например, у вегетарианцев).
- Усиленный рост кости, когда он опережает развитие сосудов.
- Избыточная функциональная нагрузка на суставы, особенно в детском и подростковом возрасте.
- Малоподвижный образ жизни (гиподинамия), приводящий к застою крови.
- Врожденные аномалии развития костно-суставной системы.
- Избыточный вес, увеличивающий нагрузку на кости и суставы.
- Наследственная предрасположенность (особенность структуры кости).
Важно! Лицам, входящим в группу риска по остеохондропатии, особое внимание следует обращать на костную систему, а при малейших жалобах обращаться к врачу.
Классификация остеохондропатии, ее виды
Остеохондропатия различается по месту локализации болезни , которая имеет 3 основных «излюбленных» места:
- эпифизы (суставные концы) трубчатых костей;
- апофизы костей (выступы, бугристости);
- короткие кости (позвонки, кости предплюсны стопы).

В области эпифизов костей развиваются следующие виды остеохондропатии :
- головки бедренной кости;
- головок плюсневых костей стопы;
- верхнего эпифиза голени;
- пальцев кисти;
- грудинного эпифиза ключицы.
Апофизарные остеохондропатии:
- большеберцовой кости голени;
- апофизов позвонков;
- пяточной кости;
- коленного сустава;
- лонной (лобковой) кости.
Изучите более подробно на нашем портале.
Остеохондропатии коротких костей:
- тел позвонков;
- ладьевидной кости стопы;
- полулунной кости запястья;
- сесамовидной (дополнительной) кости у основания 1-го пальца стопы.
Стадии развития и клинические проявления остеохондропатии
Болезнь развивается постепенно, в течение 2-3 лет, проходя следующие 3 фазы:
- Первая стадия — начальная, когда происходит омертвение (некроз) участка кости вследствие нарушения кровообращения. Проявляется болями ноющего характера в костях, суставах или позвоночнике (в зависимости от локализации), повышенной утомляемостью, нарушением движений.
- Вторая стадия — разрушение, фрагментация кости (разделение на фрагменты). Характерно усиление болей, деформация кости, появление патологических переломов (без видимой травмы). Функция нарушена значительно.
- Третья стадия — восстановление кости. Разрушенная кость постепенно восстанавливается, дефекты восполняются костной тканью, но развиваются склеротические явления, артроз близлежащих суставов. Болевой синдром уменьшается, но может остаться деформация и ограничение функции.

Фазы развития остеохондропатии: а — нарушение кровообращения, б — развитие некроза, в — образование фрагментов кости, г, д — восстановление, заживление кости
Методы диагностики
Для диагностики остеохондропатии применяются следующие методы:
- рентгенография;
- компьютерная томография (КТ);
- магнитно-резонансная томография (МРТ);
- радиоизотопное исследование всего скелета (сцинтиграфия);
- ультразвуковое сканирование (УЗИ);
- денситометрия (определение плотности кости).
Информация. При обследовании детей отдают преимущество нелучевым методам — УЗИ, МРТ.

Отдельные виды остеохондропатии, лечение
Каждый вид остеохондропатии имеет свои особенности проявления, лечебная программа также составляется индивидуально с учетом возраста и стадии болезни.
Болезнь Легга-Кальве-Пертеса
Это остеохондропатия тазобедренного сустава. Большинство больных — мальчики от 5 до 14 лет, поражение чаще одностороннее. Некроз развивается в головке бедренной кости. Заболевание проявляется болями в суставе, затруднением ходьбы, хромотой, позже атрофируются мышцы бедра, ягодиц, укорачивается конечность.

Лечение болезни требует длительного времени (2-4 года). Сустав обездвиживают, конечность изолируют от нагрузки (шина, костыли или вытяжение). Назначают препараты кальция и фосфора, витамины, сосудорасширяющие препараты, местно — ионофорез с кальцием, массаж, ЛФК. Хороший эффект дает лечение в специализированном санатории. Заболевание обычно хорошо поддается лечению, и только при его неэффективности показана операция (остеотомия, удаление некротизировавшихся участков кости, пластика сустава или эндопротезирование).
Важно. Болезнь Пертеса может привести к необратимым изменениям сустава, когда понадобится протезирование. Поэтому лечение ее должно быть своевременным и квалифицированным.
Болезнь Шляттера (Осгуда-Шляттера)
Это остеохондропатия большеберцовой кости, а точнее — ее бугристости, находящейся на передней поверхности голени, сразу под коленным суставом. Болеют как мальчики, так и девочки от 10 до 17 лет, в основном усиленно занимающиеся спортом. Ниже колена появляется болезненная припухлость, ходьба и движения в колене болезненны.
Для лечения остеохондропатии большеберцовой кости конечность фиксируют шиной, назначают физиопроцедуры, массаж, препараты кальция. Заболевание обычно хорошо поддается лечению, хотя «шишка» на кости остается.
Остеохондропатия стопы у детей
Чаще поражаются ладьевидная, пяточная, плюсневые кости. Некроз в ладьевидной кости, расположенной по внутренней стороне стопы, называется болезнью Келлера I . Заболевают в большинстве мальчики от 3 до 7 лет, поражение одностороннее. Ребенок при ходьбе начинает прихрамывать, опирается на внешний отдел стопы (кривит ножку). Обычно болезнь не дает резкой симптоматики, может остаться недиагностированной, проходит сама в течение года. При выявлении назначают ношение супинаторов, специальной обуви, физиопроцедуры, ЛФК.
Остеохондропатия головок II-III плюсневых костей (болезнь Келлера II) чаще встречается у девочек подросткового возраста, поражаются обе стопы. При ходьбе появляются боли в стопе, которые потом принимают постоянный характер, могут беспокоить даже во время сна. Появляется отек стопы, укорочение пальца. Болезнь длится 2-3 года — до тех пор, пока не прекратится усиленный рост костей. Схема лечения также включает препараты кальция, витамины, физиотерапию, массаж и ЛФК.
Остеохондропатия пяточной кости (болезнь Шинца) может развиться и у мальчиков, и у девочек в возрасте 7-12 лет, чаще поражаются обе конечности. Появляется боль, припухлость на задней поверхности пятки, хромота, затруднение ношения обуви. Ребенок начинает ходить, опираясь больше на пальцы стопы. Со временем может развиться атрофия икроножной мышцы.

Остеохондропатия пяточной кости у детей — довольно распространенное явление, длящееся довольно долго, вплоть до окончания роста костей, а уплотнение в области бугристости пяток может остаться на всю жизнь. Лечение остеохондропатии пяточной кости у детей заключается в иммобилизации стопы шиной, назначении физиопроцедур, витаминных и противовоспалительных препаратов, средств для улучшения кровообращения и микроциркуляции.
Остеохондропатия позвоночника
Чаще встречается остеохондропатия грудного отдела позвоночника, выделяют 2 ее вида:
- болезнь Шейермана-Мау, при которой деструктивный процесс происходит в эпифизах позвонков, то есть вблизи дисков;
- болезнь Кальве — поражение самих тел позвонков.
Заболевают в основном подростки и молодежь (11-19 лет). Заболевание распространено, особенно в последние десятилетия. Симптоматика выражается в деформации позвоночника (плоская или круглая спина), вогнутости грудины («грудь сапожника»), болях в спине, атрофии мышц грудной клетки, повышенной их утомляемости. Пациент не может находиться долго в вертикальном положении, выполнять физические нагрузки. Постепенно развивается клиновидная деформация позвонков, они приобретают вид трапеции (снижается высота тел в передних отделах). В дальнейшем к этим изменениям присоединяются остеохондроз и деформирующий спондилез .

Изменения тел позвонков при остеохондропатии: слева — клиновидная их деформация, справа — ее результат (кифоз спины)
Лечение остеохондропатии позвоночника длительное : физиотерапия, ЛФК, массаж, ношение корригирующего корсета, витаминотерапия, хондропротекторы, санаторное лечение. В редких случаях, когда выражена деформация позвоночника или образовались грыжи дисков, смещение позвонков, выполняют операции (коррекция и фиксация позвонков, пластика дужек и дисков).
Остеохондропатия — возрастное заболевание, поддающееся лечению. Если оно начато вовремя, проводится комплексно и квалифицированно, в большинстве случаев наступает выздоровление.
Остеохондропатия – заболевание детей и подростков, при котором в костях развивается дегенеративно-дистрофический процесс.
При остеохондропатии чаще всего поражаются пяточная, бедренная кости, апофизы позвонковых тел, бугристость большеберцовой кости.
Причины появления
На сегодня причины появления заболевания не изучены до конца, но выделяют несколько решающих факторов:
- врожденная или семейная предрасположенность;
- гормональные факторы – заболевание развивается у пациентов с патологией функции эндокринных желез;
- нарушения метаболизма незаменимых веществ. Остеохондропатию часто вызывает нарушение усваиваемости кальция, витаминов;
- травматические факторы. Остеохондропатия возникает после чрезмерных физических нагрузок, в т.ч. усиленных сокращений мышц, частых травм. Изначально эти виды нагрузок приводят к прогрессирующему сдавливанию, а после к сужению мелких сосудов губчатых костей, особенно в участках наибольшего давления.
Симптомы остеохондропатии
Остеохондропатия пяточной кости (заболевание Хаглунда-Шинца) развивается чаще всего у девочек 12-16л, характеризуется постепенно нарастающими или острыми болями в бугре пяточной кости, возникающими после нагрузки. У места прикрепления ахиллова сухожилия, над пяточным бугром отмечается припухлость. Больные начинают ходить, опираясь на носок, а занятия спортом, прыжки становятся физически невозможными.
Остеохондропатия позвоночника (заболевание Шейермана-Мау) развивается чаще всего у юношей 11-18л. Первая стадия характеризуется увеличенным грудным кифозом (искривление позвоночника в верхнем его отделе), вторая – болью в спине (особенно при продолжительной ходьбе, сидении), быстрой утомляемостью и слабостью спинных мышц, увеличением грудного кифоза. На третьей стадии остеохондропатии позвоночника наблюдается полное слияние апофизов с позвонками. Со временем развивается остеохондроз с нарастающим болевым синдромом.
Остеохондропатия бедренной кости (заболевание Легга-Кальве-Пертеса) развивается в большинстве случаев у мальчиков 4-12л. В начале болезни жалоб нет, после появляются боли в тазобедренном суставе, отдающие в колено. Возникают боли после нагрузки и проходят после отдыха, поэтому дети не всегда на них жалуются. Постепенно ограничиваются движения тазобедренного сустава, развивается атрофия мышц, и бедро с больной стороны худеет.
Остеохондропатия бугристости большеберцовой кости (заболевание Шлаттера) развивается у мальчиков 12-16л, особенно у тех, кто занимается балетом, спортивными танцами, спортом. Пациент жалуется на боли под надколенником, припухлость. При напряжении четырехглавой бедренной мышцы, при приседании, подъеме по лестнице боль усиливается.
Диагностика заболевания
Для определения остеохондропатии пяточной кости основываются на клинических данных и результатах рентгенологического обследования (отмечается фрагментация, уплотнение апофиза, «шероховатости» на бугре пяточной кости). Проводится также дифференциальная диагностика остеохондропатии с пяточной шпорой (у более взрослых пациентов), ахиллобурситом.
Диагностирование остеохондропатии позвоночника происходит на основании данных осмотра (усилен грудной кифоз) и рентгенологического обследования (на снимках видно, что форма позвонков изменена – они приобретают клиновидную форму).
 Остеохондропатия бедренной кости также определяется по рентгенологическим снимкам. Выделено пять стадий изменения головки бедренной кости.
Остеохондропатия бедренной кости также определяется по рентгенологическим снимкам. Выделено пять стадий изменения головки бедренной кости.
Лечение остеохондропатии
Терапия остеохондропатии пяточной кости заключается в назначении нестероидных противовоспалительных средств (если донимают сильные боли), физиотерапевтических процедур, в уменьшении физических нагрузок. Для снятия нагрузки на пяточную кость используют специальные стельки-супинаторы.
Остеохондропатию позвоночника лечат с помощью массажа, плавания, подводного вытягивания, лечебной физкультуры. В отдельных случаях при сильном нарушении осанки назначают операцию.
Лечение остеохондропатии бедренной кости может быть оперативным и консервативным. Различные костно-пластические операции назначаются в зависимости от стадии болезни. Консервативное лечение остеохондропатии заключается в соблюдении постельного режима (пациенту нельзя сидеть), проведении массажа ног, физиотерапевтических процедур. Практикуют скелетное вытягивание за оба бедра.
Для лечения остеохондропатии бугристости большеберцовой кости назначают физиотерапевтические процедуры, тепло. Если боль сильная, накладывают гипсовую повязку. Иногда прибегают к операции – удаляют фрагмент бугристости. Нагрузки на четырехглавую бедренную мышцу исключены.
Профилактика заболевания
Для профилактики остеохондропатии пяточной кости рекомендуют носить свободную обувь.
Профилактика остеохондропатии позвоночника заключается в занятиях лечебной физкультурой для создания мышечного корсета. Усиленные физические нагрузки необходимо ограничить. Ношение корсета при данном заболевании неэффективно.
Хорошей профилактикой остеохондропатии бедренной кости служит массаж, плавание.
Для предупреждения остеохондропатии бугра большеберцовой кости спортсменам во время тренировок рекомендуют вшивать в форму поролоновые подушки 2-4см толщиной.
Видео с YouTube по теме статьи:
Болезнь Пертеса (или остеохондропатия головки бедра) относится к числу наиболее часто встречающихся заболеваний тазобедренного сустава у детей в возрасте от 3 до 14 лет и представляет собой самую распространенную в детском возрасте разновидность асептического некроза головки бедренной кости.
Термин «асептический некроз» в данном случае означает омертвение костной ткани эпифиза (то есть верхней полусферы) головки бедра неинфекционной природы (рис. 1).
Рис. 1. Анатомическое строение тазобедренного сустава (Р.Д. Синельников. "Атлас нормальной анатомии человека". 1967):
1. Эпифиз головки бедра.
2. Шейка бедра.
3. Вертлужная впадина.
4. Большой вертел.
5. Малый вертел.
6. Суставная капсула.
Заболеванию в большей степени подвержены мальчики 5-12 лет, однако у девочек оно протекает более тяжело. Патологический процесс имеет несколько стадий и может продолжаться в течение многих месяцев, примерно в 5% случаев поражаются оба тазобедренных сустава.
Взгляды разных исследователей на этиологию и патогенез (то есть происхождение и развитие) болезни Пертеса до настоящего времени расходятся. Наиболее распространенная патогенетическая теория заболевания в «компактном» и упрощенном виде представлена в нижеследующем.
Обязательным условием развития болезни Пертеса является наличие у ребенка определенных предрасполагающих (врожденных) и производящих (приобретенных) факторов. Предрасполагающим фактором болезни Пертеса (или фоном для её появления) служит так называемая миелодисплазия поясничного отдела спинного мозга, отвечающего за иннервацию тазобедренных суставов.
Термин «миелодисплазия» означает нарушение развития (в данном случае - недоразвитие) спинного мозга. Недоразвитие спинного мозга носит врожденный - наследственно обусловленный характер, оно встречается у значительной части детей и различается по степени тяжести. Миелодисплазия легкой степени может оставаться незамеченной на протяжении всей жизни, в то время как более существенные нарушения развития спинного мозга проявляются в виде целого ряда ортопедических заболеваний, к которым относится и болезнь Пертеса.
Анатомическое строение области тазобедренных суставов у детей с миелодисплазией отличается в частности тем, что количество и калибр сосудов и нервов, осуществляющих иннервацию и кровоснабжение суставов, меньше, чем у здорового ребенка (рис. 2).

Рис. 2. Кровоснабжение головки и шейки бедра (G.H. Thompson, R.B. Salter. "Legg-Calve-Perthes Disease". 1986):
1. Наружная и внутренняя артерии, огибающие бедренную кость.
2. Восходящие ветви огибающих артерий, входящие в шейку и головку бедра.
3. Хрящевая зона роста головки бедра.
Предельно упрощенно данную ситуацию можно представить следующим образом - вместо 10-12 относительно крупных артерий и вен, входящих и выходящих из головки бедра, у больного имеются 2-4 мелкие (врожденно недоразвитые) артерии и вены, поэтому кровоток в тканях сустава хронически понижен, и они испытывают дефицит питания. Наличие миелодисплазии также отрицательно влияет и на тонус сосудистой стенки.
Между тем, болезнь Пертеса развивается только в том случае, когда кровоснабжение головки бедра полностью прекращается, что происходит под действием так называемых производящих факторов. Производящими факторами болезни Пертеса чаще всего являются воспаление тазобедренного сустава или незначительная по силе травма, ведущие к компрессии (пережатию) вышеописанных малочисленных и недоразвитых сосудов извне. Воспаление тазобедренного сустава (в данном случае - транзиторный синовит) возникает под влиянием инфекции, попадающей в сустав, например, из носоглотки при простудных заболеваниях. Именно поэтому последние нередко предшествуют началу болезни Пертеса, что отмечают сами родители. Незначительная по силе травма, например, в результате прыжка со стула, или просто неловкое движение может остаться незамеченной как родителями, так и детьми. В результате происходит полное блокирование кровотока (или инфаркт) головки бедра, приводящий к её частичному или полному омертвению, то есть образованию очага некроза (рис. 3).

Рис. 3. Рентгенограмма тазобедренного сустава ребенка с болезнью Пертеса (Perthes):
1. Очаг некроза в головке правой бедренной кости.
Клинические проявления заболевания на данном этапе очень скудны или вообще отсутствуют. Чаще всего дети периодически жалуются на незначительные по выраженности болевые ощущения в области бедра, коленного или тазобедренного сустава. Родители могут заметить некоторые нарушения походки в виде «припадания» на одну ногу или «приволакивания» ноги. Сильные боли отмечаются гораздо реже, грубой хромоты, как правило, не бывает - поэтому обращение к врачу в первой стадии заболевания (стадия остеонекроза) является довольно большой редкостью.
В дальнейшем омертвевшая костная ткань верхней полусферы головки бедра теряет свою нормальную механическую прочность, вследствие чего, под влиянием обычной повседневной нагрузки - ходьба, прыжки и т.п. или даже при отсутствии таковой, постепенно развивается деформация головки бедра, которая является главной и наиболее сложной проблемой в лечении ребенка (рис. 4).

Рис. 4. Седловидная деформация головки бедра у ребенка с болезнью Пертеса (Perthes):
А. Схема тазобедренного сустава.
Б. Артропневнограмма тазобедренного сустава.
На момент завершения болезни Пертеса деформация головки бедра может иметь разную степень выраженности - от незначительной и едва заметной на рентгенограмме до грубой «грибовидной» или «седловидной». Степень деформации головки бедра определяется размерами и локализацией (расположением) очага некроза в эпифизе и, в свою очередь, напрямую определяет исход заболевания - благоприятный или неблагоприятный. Неблагоприятным исходом заболевания считается появление клинических признаков так называемого деформирующего коксартроза (неуклонно прогрессирующие дегенеративные изменения сустава) в виде выраженного болевого синдрома и нарушения походки в том возрасте, когда необходимо устраивать личную жизнь и получать образование. Под благоприятным исходом подразумевается ситуация, когда сустав функционирует многие годы до пожилого возраста, не давая о себе знать.
Однако, по данным современных исследований, первая стадия заболевания является обратимой, это означает, что при благоприятном стечении обстоятельств (небольшой объем очага некроза и быстрое восстановление кровотока в эпифизе) заболевание может завершиться до начала развития деформации головки бедра, не переходя во вторую стадию. Появление рентгенологических признаков начавшейся деформации головки бедра свидетельствует о переходе болезни в стадию импрессионного перелома и начале необратимого и продолжительного многостадийного патологического процесса.
За время течения заболевания строение головки бедра претерпевает значительные изменения - после уплощения во второй стадии, она подвергается фрагментации (третья стадия), то есть имеющийся очаг некроза «распадается» на несколько отдельных частей в результате врастания в него соединительной ткани, содержащей сосуды и нервы (рис. 5).

Рис. 5. Картина болезни Пертеса в стадии фрагментации (G.H. Thompson, R.B. Salter. "Legg-Calve-Perthes Disease". 1986):
1. Фрагменты эпифиза головки бедра.
Постепенно над процессами «разрушения» начинают преобладать процессы репарации (заживления), которые заключаются в новообразовании костной ткани в очаге некроза - на смену стадии фрагментации приходит стадия восстановления. Новообразованная костная ткань в результате продолжающейся перестройки со временем приобретает балочное строение и архитектонику, приближающиеся к нормальным (стадия исхода), однако, механическая прочность кости остается сниженной.
Помимо новообразования костной ткани в очаге некроза, стадия восстановления характеризуется возобновлением роста головки бедра. При большом объеме очага некроза и отсутствии адекватного лечения рост головки бедра является причиной прогрессирования деформации. Головка бедра, будучи до начала заболевания сферичной (выпуклой), становится плоской или вогнутой, её передне-наружный квадрант может значительно выстоять из суставной впадины, поэтому не редко имеет место подвывих в тазобедренном суставе (рис. 6).

Рис. 6. Схема формирования деформации и подвывиха головки бедра в результате продолжающегося роста при отсутствии лечения (K.-P. Schulitz, H.-O. Dustmann. "Morbus Perthes". 1998).
Возникает несоответствие формы суставных поверхностей вертлужной впадины, сохраняющей сферичность, и головки бедра, что играет решающую роль в судьбе пораженного сустава.
Головка бедра ребенка содержит хрящевую зону роста - это та часть бедренной кости, за счет которой последняя растет в длину (рис 2). При обширных очагах некроза в эпифизе зона роста вовлекается в патологический процесс, полностью или частично разрушаясь. В результате с годами формируется деформация всего верхнего конца бедренной кости, характеризующаяся укорочением шейки бедра и высоким стоянием большого вертела, и укорочение нижней конечности, которые являются причинами нарушения походки (рис. 7).
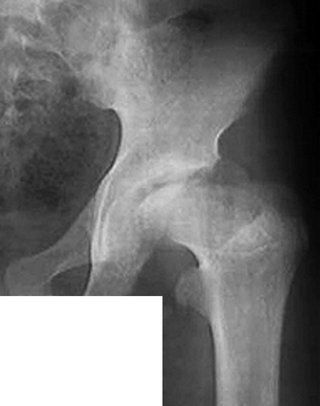
Рис. 7. Типичная деформация проксимального конца бедренной кости при болезни Пертеса.
К счастью, у большинства детей с болезнью Пертеса (не менее, чем две трети случаев заболевания) очаг некроза в головке бедра имеет небольшие размеры и не включает в себя наружный отдел эпифиза и его ростковую зону, поэтому развитие выраженной деформации головки бедра и значительного несоответствия формы суставных поверхностей исключается. При этом деформация верхнего конца бедренной кости в целом и укорочение конечности также выражены незначительно.
Появление болей в бедре, коленном или тазобедренном суставе, а также нарушение походки являются поводом для обращения к врачу-ортопеду, который после выяснения анамнеза (истории появления и развития) заболевания и клинического осмотра ребенка назначает рентгенограммы тазобедренных суставов в прямой проекции и проекции Лауэнштейна (рис. 8).

Рис. 8. Необходимый минимум рентгенологического исследования при подозрении болезни Пертеса:
А. Рентгенограмма тазобедренного сустава в передне-задней проекции.
Б. Рентгенограмма тазобедренного сустава в проекции Лауэнштейна.
Это необходимый минимум обследования, который позволяет с высокой точностью подтвердить наличие болезни Пертеса даже в первой стадии или исключить данное заболевание. В подобных случаях может быть также рекомендовано выполнение магнитно-резонансной томографии и ультразвукового исследования тазобедренных суставов, однако последние проводятся только в качестве дополнительных методов исследования, поскольку не являются определяющими в постановке диагноза болезни Пертеса.
Существуют некоторые патологические состояния, которые по своим клиническим проявлениям напоминают начало болезни Пертеса, но являются гораздо более благоприятными в плане прогноза и менее обременительными в плане лечения. К таким заболеваниям относятся в частности нейродиспластическая коксопатия и инфекционно-аллергический артрит тазобедренного сустава. При лечении по поводу данных болезней не требуется хирургического вмешательства, длительного исключения опоры на ноги и ходьбы, а также использования ортопедических приспособлений.
В основе нейродиспластической коксопатии, как и в случае с болезнью Пертеса, лежит дисплазия пояснично-крестцового отдела позвоночника и спинного мозга, обусловливающая снижение притока артериальной и оттока венозной крови в области тазобедренного сустава и нарушение его иннервации. На рентгенограммах имеются признаки дистрофии (нарушения питания) костной ткани тазового и, преимущественно, бедренного компонентов. Принципиальным отличием от болезни Пертеса является отсутствие полного блокирования кровотока (инфаркта) и, следовательно, формирования очага некроза в головке бедра.
Инфекционно-аллергический артрит (или транзиторный синовит) - воспаление внутренней (синовиальной) оболочки тазобедренного сустава, связанное с появлением и кратковременным пребыванием в суставе инфекционного агента, принесенного из других органов (очагов инфекции) с током крови, и характеризующееся нарушением кровотока той или иной степени, но также без полного блокирования и формирования очага некроза.
При постановке диагноза болезни Пертеса врач обязательно полностью исключает опору на «больную» ногу - в зависимости от возраста ребенка и его развития назначается строгий постельный режим или полупостельный режим с возможностью ограниченной ходьбы на костылях. Такие же меры предпринимаются при подозрении на болезнь Пертеса на время обследования до постановки окончательного диагноза. Необходимо поддерживать определенное положение в постели - на спине и на животе с умеренным разведением ног, положение на боку (как на «больном», так и на «здоровом») не желательно. Ребенку разрешается присаживаться в постели с опорой под спину и ограниченно сидеть. При наличии воспалительных явлений в суставе, часто сопутствующих болезни Пертеса, и связанного с ними ограничения амплитуды движений бедра, в качестве первого этапа лечения больному обязательно назначается противовоспалительная терапия.
Основной задачей лечения детей с болезнью Пертеса является приближение анатомического строения пораженного тазобедренного сустава к нормальному (исходному), только в этом случае можно надеяться на то, что в течение последующих лет жизни у пациента не будет отмечаться выраженных нарушений походки и болевых ощущений. При этом наиболее важным считается восстановление формы головки бедра (круглая головка), которая должна соответствовать форме вертлужной впадины и профилактика формирования (или устранение) подвывиха в пораженном суставе.
В основе лечения детей с болезнью Пертеса традиционно лежат консервативные мероприятия - лечебная гимнастика, массаж, физиотерапевтические процедуры, а также медикаментозная терапия, которые проводятся после обеспечения центрации головки бедра (то есть полного «погружения» её в вертлужную впадину) за счет использования одного из ортопедических приспособлений. К таким приспособлениям относятся функциональные шины (шина Мирзоевой или шина Виленского), гипсовые повязки (повязка-распорка Ланге или кокситная повязка) и различные виды вытяжения за бедро или голень (лейкопластырное, скелетное или манжеточное) и другие устройства (рис. 9).

Рис. 9. Ортопедические приспособления, используемые для лечения детей с болезнью Пертеса:
А. Гипсовая повязка-распорка по Ланге.
Б. Шина д.м.н. профессора И.И. Мирзоевой.
Все эти приспособления должны придавать «больной» ноге постоянное (на протяжении всего срока лечения) положение отведения и внутренней ротации или, по крайней мере, только отведения, которое и обеспечивает центрацию в пораженном суставе.
Постоянное поддержание положения центрации (или полного «погружения») головки бедра в вертлужной впадине является обязательным условием при лечении по поводу болезни Пертеса с большим очагом некроза, потому что в этом случае только при помощи центрации можно остановить прогрессирование деформации и развитие подвывиха головки бедра. Помимо этого, полное «погружение» головки бедра в суставную впадину обеспечивает оптимальные условия для исправления деформации, которая уже имелась на момент начала лечения. Использование консервативных методов лечения, не предусматривающих центрацию головки бедра, допустимо только в том случае, когда очаг некроза имеет небольшие размеры и включает в себя только передний или передний и центральный отделы эпифиза, а ребенок относится к младшей возрастной группе. При этом врач, назначая контрольные рентгенограммы, постоянно убеждается в том, что размеры очага некроза не увеличились.
Лечебная гимнастика проводится с целью стимуляции репаративного процесса (заживления) в головке бедра и увеличения амплитуды движений в пораженном суставе, она возможна только при использовании съемных центрирующих приспособлений, в то время как в условиях скелетного вытяжения или гипсовых повязок проведение упражнений в значительной степени ограничено. Тонизирующий массаж и электростимуляция мышц, окружающих тазобедренный сустав, позволяет поддерживать их функциональную активность и препятствовать прогрессированию гипотрофии (уменьшение мышечного объема), являющейся одним из неотъемлемых клинических проявлений болезни Пертеса и характерной для длительного постельного режима.
Важным компонентом комплексного консервативного лечения является использование медикаментозных препаратов и физиотерапевтических приборов ангиопротективного действия на фоне которых назначаются остеопротекторы и хондропротекторы. Подобные приборы и препараты (ангиопротекторы) обеспечивают улучшение притока артериальной и оттока венозной крови в области тазобедренного сустава, в то время как препараты остео- и хондропротективного действия стимулируют новообразование костной ткани в очаге некроза и положительно влияют на строение хрящевой ткани, образующей суставные поверхности. Данные препараты обычно назначаются в виде электрофореза на область пояснично-крестцового отдела позвоночника и пораженного сустава, а также в виде форм для приема внутрь (капсулы, таблетки, порошки) и внутримышечных инъекций. Выраженным остеопротективным действием обладают в частности микроэлементы - кальций, фосфор и сера, которые назначаются, как правило, в виде электрофореза по трех- или двухполюсной методике, в комбинации друг с другом или с аскорбиновой кислотой. Микроэлементы могут быть назначены также в виде теплых (минеральных) грязей или ванн, имеющихся чаще всего в условиях санатория. Среди физиотерапевтических приборов, способствующих нормализации кровотока в глубине тканей, большое распространение получил «Витафон», оказывающий виброакустическое воздействие на сосудистую стенку.
Перечисленные лечебные мероприятия назначаются курсами продолжительностью от двух до четырех недель с перерывами не менее одного месяца - обычно проводится четыре или пять курсов массажа и физиопроцедур в год. Исключением является лечебная гимнастика, которая выполняется ежедневно (обычно два раза в сутки) на протяжении всего срока лечения и при необходимости сочетается с укладками бедра. Кроме того, желательно включение в план лечения плавания в бассейне - не более двух раз в неделю, а в стадии восстановления - велотренажера. Тепловые процедуры (парафин, озокерит и горячие грязи), температура которых составляет более 40°С, считаются противопоказанными, так как способствуют затруднению оттока венозной крови и связанному с этим повышению внутрикостного давления, замедляющему течение репаративного процесса. Детям, получающим лечение по поводу болезни Пертеса, показано санаторно-курортное лечение. Курорты ортопедического профиля имеются во многих регионах России - в Новгородской области («Старая Русcа»), в Калининградской области («Пионерск»), в Рязанской области («Кирицы»), а также на Черноморском побережье (Геленджик, Анапа, Евпатория).
Продолжительность рассматриваемого консервативного лечения, проводящегося в условиях полного, а затем частичного исключения опоры на «больную» ногу, составляет в среднем два с половиной года - от одного до четырех лет. Она зависит главным образом от возраста ребенка на момент начала заболевания, стадии патологического процесса на момент начала лечения и объема очага некроза в головке бедра. Поэтому подобное лечение показано чаще всего детям младшей возрастной группы (до 6-ти лет) с небольшим очагом некроза. Сроки начала дозированной опорной нагрузки на больную ногу, а затем и ходьбы без подручных средств, определяются врачом-ортопедом на основании данных рентгенографии тазобедренных суставов, проводящейся не чаще, чем один раз в три или четыре месяца, или магнитно-резонансной томографии.
Помимо большой продолжительности и связанных с ней изоляцией ребенка от сверстников и отставания в физическом развитии, отрицательной стороной консервативного лечения является появление у многих детей избыточного веса, который в последующем становится причиной постоянной перегрузки пораженного сустава. В связи с этим лечение проводится на фоне специальной диеты и обязательно включает допустимую физическую нагрузку. Но основным недостатком консервативного лечения является, пожалуй, необходимость постоянного поддержания правильного положения в постели и использование вышеупомянутых центрирующих приспособлений, доставляющих значительные неудобства детям и их родителям. Между тем, использование ортопедических шин, различных видов вытяжения или гипсовых повязок во многих случаях относится к обязательным и абсолютно необходимым условиям проведения лечения.
Преимуществом консервативного лечения является отсутствие необходимости выполнения хирургического вмешательства, и связанных с ним мероприятий, к которым относятся общее обезболивание (наркоз), перевязки операционной раны и снятие швов, внутримышечные инъекции аналгетиков и антибиотиков, а в ряде случаев и переливание крови. Ожидание операции может стать серьёзным стрессом для ребенка, а ранний послеоперационный период связан с болевыми ощущениями.
Тем не менее, в некоторых, наиболее тяжелых, случаях болезни Пертеса вместо использования центрирующих ортопедических приспособлений предпочтительно выполнение реконструктивно-восстановительного хирургического вмешательства на тазобедренном суставе. Последнее обеспечивает полное «погружение» головки бедра в вертлужную впадину не за счет придания нижней конечности определенного положения, а за счет одномоментного изменения пространственного положения тазового или бедренного компонента сустава после пересечения соответствующей (тазовой или бедренной) кости. Поэтому в послеоперационном периоде ребенок избавлен от многомесячного ношения ортопедических шин или пребывания в условиях вытяжения. Важным положительным эффектом подобных операций является также стимуляция репаративного процесса в очаге некроза и, следовательно, сокращение сроков лечения пациента.
Хирургическое вмешательство включается в план лечения только в случаях болезни Пертеса у детей в возрасте не менее 6-ти лет с большим очагом некроза, являющимся причиной развития выраженной деформации, а, нередко, и подвывиха головки бедра. Рассматриваемые случаи характеризуются также длительными сроками течения заболевания - без операции ребенок может лечиться три года и даже до пяти лет. К сожалению, частота тяжелых случаев болезни Пертеса в последние годы значительно возросла.
Типичными реконструктивно-восстановительными хирургическими вмешательствами, применяющимися для лечения детей с болезнью Пертеса в мировой практике, являются корригирующая медиализирующая остеотомия бедра и ротационная транспозиция вертлужной впадины по Солтеру (Salter), отличающиеся относительно небольшой травматичностью и продолжительностью не более одного часа (рис. 10).

Рис. 10. Анатомическое строение тазобедренного сустава у ребенка с болезнью Пертеса (к.м.н. Д.Б. Барсуков, к.м.н. И.Ю. Поздникин "Хирургическое лечение детей с болезнью Легга-Кальве-Пертеса):
А. До хирургического лечения.
Б. После выполнения корригигурующей (варизирующей) медиализирующей остетотомии бедра.
В. После выполнения ротационной транспозиции вертлужной впадины по Солтеру (Salter).
1. Металлоконструкции.
2. Линии остетомий (пересечения) тазовой и бедренной костей.
Вмешательства большего объема используются значительно реже. При выполнении данных операций фрагменты костей фиксируются в положении коррекции специальными металлоконструкциями, которые удаляются обычно спустя несколько месяцев. На операционном столе ребенку накладывается гипсовая повязка той или иной разновидности - в зависимости от характера проведенного вмешательства, срок пребывания в ней составляет четыре или пять недель.
Помимо сокращения сроков исключения опоры на «больную» ногу, которые составляют в среднем 12 месяцев (от 9 до 15 месяцев), серьезным преимуществом хирургического лечения является более полное восстановление высоты пораженной головки бедра и, следовательно, её формы в целом.
Большое влияние на прогноз заболевания, безусловно, оказывает качество проведенного хирургического вмешательства. Вероятность успешного завершения операции значительно возрастает, если больной оперируется хирургами, специализирующимися на патологии детского тазобедренного сустава и проводящими подобные операции часто. Скорее всего, таких специалистов можно встретить в специализированных отделениях патологии тазобедренного сустава научно-исследовательских институтов или в детских ортопедических отделениях областных, республиканских и краевых больниц.
Не меньшее влияние на прогноз заболевания оказывает добросовестность выполнения самим ребенком и его родителями рекомендаций по дальнейшему (послеоперационному) лечению данных врачом-ортопедом. Главными из них являются исключение избыточной физической нагрузки (прыжков, бега, поднятия тяжестей) и избыточного веса тела на протяжении всей последующей жизни. В связи с этим ребенку запрещаются занятия практически всеми видами спорта и занятия физкультурой в школе - в лучшем случае разрешается посещение спецгруппы без сдачи нормативов. Физическая активность подобных детей должна проявляться в виде некоторых допустимых видов нагрузки - регулярное плавание в бассейне, лечебная гимнастика для поддержания нормальной амплитуды движений в суставе, занятия на велотренажере и спортивный велосипед. В противном случае, развивающаяся гиподинамия практически всегда приводит к появлению избыточного веса, что становится серьезной дополнительной проблемой для пациента. Для поддержания нормального веса нередко требуется соблюдение специальной диеты, а иногда и медикаментозное лечение по согласованию с врачом-эндокринологом.
Трудно переоценить правильность трудоустройства людей, перенесших болезнь Пертеса - выбранная профессия не должна быть связана с тяжелой физической нагрузкой и даже постоянным (в течение всего рабочего дня) пребыванием на ногах. Важным является регулярность проведения поддерживающих курсов восстановительного лечения (физио- и медикаментозная терапия), в том числе в условиях санаториев.
Пренебрежение перечисленными рекомендациями, даже при наилучших ближайших результатах лечения, приводит к появлению клинических признаков деформирующего коксартроза в виде болевого синдрома и нарушения походки. Обычно при болезни Пертеса клинические симптомы коксартроза появляются относительно поздно в сравнении с другими, более тяжелыми, заболеваниями тазобедренного сустава или не появляются вообще. Однако в случаях, когда пациент забывает о том, что сустав надо беречь, они могут развиться и в молодом возрасте, тогда, в зависимости от выраженности болевого синдрома, принимается решение об эндопротезировании тазобедренного сустава (замена непригодного к функции собственного органа на искусственный). Операция эндопротезирования в молодом возрасте является крайне нежелательной - она должна проводиться как можно позже. К счастью, далеко не все люди получавшие лечение по поводу болезни Пертеса нуждаются в эндопротезировании. Тоже можно сказать и о хирургических вмешательствах, направленных на уравнивание длины нижних конечностей - большая разница в длине ног встречается не часто.
Таким образом, определяющими обстоятельствами в прогнозе болезни Пертеса являются возраст ребенка на момент начала патологического процесса, размеры и расположение очага некроза в головке бедра, ранняя диагностика заболевания и адекватность проводимых лечебных мероприятий. Поэтому появление у ребенка даже незначительных болей в ногах или нарушения походки - это повод для обращения к врачу-ортопеду. Правильный выбор места лечения и добросовестность выполнения врачебных рекомендаций обеспечивают благоприятный исход болезни Пертеса даже в наиболее тяжелых случаях заболевания.
Частота от 0,18 до 3%. По данным ЦИТО, указанная патология наблюдается у 2,7% ортопедических больных, при этом наиболее часто поражаются головка бедренной кости, бугристость большеберцовой кости и апофизы тел позвонков (81,7% от всех остеохондропатии).
Остеохондропатии
заболевания, встречающиеся преимущественно в детском и юношеском возрасте и характеризующиеся поражением субхондральных отделов эпифизов некоторых костей. Для этих заболеваний характерно хроническое течение и благоприятный исход.
Этиология. Теории: врожденная, нарушения обмена, инфекционная, хронические травмы, перегрузки и др.
Важным фактором патогенеза остеохондропатий является асептический остеонекроз, который развивается в результате местного нарушения артериального кровоснабжения кости. Доказана роль аутосомно-доминантного наследования в возникновении большинства видов остеохондропатий. Конкретные механизмы ишемии эпифизов пока не раскрыты.
Патологическая анатомия. Различают пять стадий заболевания
1. Асептического некроза. Происходит некроз губчатого вещества и костного мозга. Хрящевой покров остается жизнеспособным.
2. Импрессионного перелома . Эпифиз пораженной кости деформируется под влиянием нагрузки.
3. Рассасывания. Некротизированные ткани рассасываются и прорастают соединительной тканью.
4. Репарации. Пораженный эпифиз замещается новообразованной костью.
5. Конечная. Характеризуется вторичными изменениями (нарушение формы головки, деформирующий артроз). Причиной деформаций является предшествующий иммпрессионный перелом. Структура костной ткани восстанавливается полностью.
Классификация остеохондропатий (С.А. Рейнберг, 1964)
Остеохондропатии эпифизарных концов трубчатых костей (головки бедренной кости (болезнь Легг-Кальве-Пертеса), головки II и III плюсневых костей (вторая болезнь А.Келера), грудинного конца ключицы (болезнь Фридриха);
Остеохондропатии коротких губчатых костей (надколенника, ладьевидной кости стопы (первая болезнь А.Келера), полулунной кости кисти (болезнь Кинбека), тела позвонка (болезнь Кальве), сесамовидной кости I плюсне-фалангового сустава (болезнь Ренандер-Мюллера), ладьевидной кости кисти (болезнь Прайзера);
Остеохондропатии апофизов (бугристости большеберцовой кости (болезнь Осгуд-Шлаттера), бугра пяточной кости (болезнь Шинца), апофизов позвонков (болезнь Шойэрмана-Мау - юношеский кифоз), лонной кости (болезнь Ван Нека);
Частичные остеохондропатии суставных поверхностей (болезнь Кенига)
Чаще в возраст от 5 до 12 лет, Мальчики страдают в 4-5 раз чаще, чем девочки. Процесс в большинстве случаев бывает односторонним.
Клиника. Ноющая боль, хромота, гипотрофия мышц, а в далеко зашедших случаях - функциональное укорочение нижней конечности на 1-2 см и ограничение подвижности в тазобедренном суставе.
Остеохондропатия головки бедренной кости (болезнь Легг-Кальве-Пертеса)
I стадия – асептического некроза, которая продолжается от 2 до 6 мес - рентгенологические проявления отсутствуют (субхондральный некроз губчатого вещества).
Остеохондропатия головки бедренной кости (болезнь Легг-Кальве-Пертеса)
II стадия – остеохондрит и импрессионный перелом эпифиза головки бедра. (длительность до 6 мес) головка бедренной кости равномерно затемнена и лишена структурного рисунка. Происходит сминание головки, суставная щель расширяется.
Остеохондропатия головки бедренной кости (болезнь Легг-Кальве-Пертеса)
III стадия – фрагментация костной ткани, (продолжительность от 1,5 до 2,5 лет) головка разделена на отдельные фрагменты неправильной формы и значительно уплощена. Суставная щель расширена.
Остеохондропатия головки бедренной кости (болезнь Легг-Кальве-Пертеса)
IV стадия – перестройка специфической балочной структуры костной ткани головки бедра, (длительность от 0,5 до 1,5 лет) головка бедра имеет неровные контуры, ее структура постепенно восстанавливается.
V стадия – исход: выздоровление или развитие деформирующего артроза, может принять грибовидную форму
В основе консервативного лечения лежит ранняя и длительная разгрузка конечности, что позволяет сохранить форму головки бедренной кости. Назначают постельный режим с накожным или скелетным вытяжением за больную ногу, ходьбу на костылях без нагрузки на больную конечность. Разгрузка не должна исключать движения в суставе, поэтому для укрепления мышц тазобедренного сустава и всей нижней конечности назначают лечебную физкультуру, плавание в бассейне, массаж.
С целью улучшения репаративных процессов назначают медикаментозное лечение и физиотерапевтические процедуры.
Если болезнь Пертеса развивается в диспластическом суставе, то основным методом лечения у этих больных должен быть оперативный, направленный на создание оптимальных условий в тазобедренном суставе (внесуставная реконструкция сустава с ликвидацией дефицита покрытия головки бедра в результате дисплазии).
Хирургические вмешательства при остеохондропатии головки бедра позволяют сократить сроки лечения заболевания в 1,5 раза и способствуют снижению инвалидизации данной категории больных.
Остеохондропатия бугристости большеберцовой кости
(болезнь Осгуда-Шлаттера)
В научной литературе известно как асептический некроз бугристости большеберцовой кости, апофизит большеберцовой кости, болезнь Ланелонга-Осгуда-Шлаттера.
Чаще болеют мальчики в возрасте от 13 до 15-18 лет. Нередко встречается двусторонняя локализация процесса. В основе заболевания лежит нарушение процессов окостенения бугристости большеберцовой кости. Остеохондропатия часто развивается без видимой причины, однако, иногда удается установить связь с повторной травмой или повышенной функцией четырехглавой мышцы бедра (например, при занятиях спортом или балетом).
Клиника. Отмечается припухлость и локальная боль в области бугристости большеберцовой кости, усиливающаяся при пальпации. Больные нередко говорят, что у них «…растет новая коленная чашечка». Зачастую определяется выраженное увеличение апофиза большеберцовой кости (в 2 раза и более). Движения в коленном суставе болезненны, особенно после физической нагрузки. Самая резкая боль возникает при «стоянии на коленках». Крайняя степень сгибания конечности в коленном суставе сопровождается выраженными болевыми ощущениями, нередко сохраняющимися и в состоянии покоя.
При рентгенологической диагностике болезни Осгуда-Шлаттера необходимо иметь в виду множество вариантов нормальной оссификации апофиза большеберцовой кости. Чаще всего апофиз окостеневает в виде хоботообразного отростка в возрасте 10-13 лет, но встречаются варианты с добавочными мелкими ядрами окостенения. Слияние апофиза с метафизом происходит к 16-18 годам.
При диагностике всегда следует учитывать несоответствие между значительным выбуханием бугристости при клиническом исследовании и почти нормальными размерами апофиза на рентгенограмме. Предпочтение необходимо отдавать клиническим данным.
Заболевание продолжается около года, а иногда и несколько лет, и заканчивается восстановлением структуры апофиза. Функция коленного сустава, как правило, не страдает.
Лечение, прежде всего, требует исключения всяких перегрузок и создания относительного покоя, вплоть до кратковременной иммобилизации, и основано на физиотерапевтических методах (магнитотерапия, электрофорез с кальцием и новокаином, бальнеотерапия и грязелечение). Оперативное лечение, как правило, не применяется, за исключением единичных случаев отрыва бугристости при повышенной физической нагрузке.
Остеохонд ропатия апофизов тел позвонков
(болезнь Шойермана-Мау)
Остеохондропатия апофизов тел позвонков или болезнь Шойерманна-Мау (юношеский кифоз) встречается чаше у юношей в период роста организма в возрасте 11-18 лет. Относится к довольно распространенному заболеванию детского возраста, составляя от 0,42 до 3,7%.
Основой остеохондропатии позвоночника считают врожденную неполноценность дисков и недостаточную прочность замыкательных пластинок тел позвонков.Отмечают влияние гормональных факторов (заболевание нередко сочетается с эндокринными расстройствами), а также наследственную предрасположенность (возможно наследование по аутосомно-доминантному типу). В прогрессировании деформации немаловажную роль играет фактор нагрузки (неправильный режим, долгое сидение в согнутом положении, тяжелая физическая работа, перенос грузов на спине, избыточные нагрузки на позвоночник при его росте при занятиях спортом).
Как показывают рентгенологические исследования нормального позвоночника, в возрасте 10-12 лет в межпозвонковых хрящевых дисках появляются добавочные апофизарные точки окостенения тела позвонка, имеющие треугольную форму на рентгенограмме в боковой проекции. Процесс их костного слияния начинается в возрасте 14-15 лет, а в 18-20 лет заканчивается. В результате тело позвонка из двояковыпуклой формы, характерной для детского возраста, превращается в двояковогнутую, которая присуща взрослому человеку.
Нарушение энхондральной оссификации в области зон роста тел позвонков (апофизарных зон) при болезни Шойерманна-Мау и приводит к возникновению их клиновидной деформации и формированию кифоза. Чаще поражаются 3-4 средних или нижнегрудных позвонка. Наиболее типично вовлечение в патологический процесс VII, VIII, IX и X грудных позвонков.
Клиника заболевания отличается медленным развитием и в течение ряда лет проходит 3 стадии.
1 стадия продолжается до появления оссификации апофизов тел позвонков и характеризуется несколько увеличенным грудным кифозом.
Во время // стадии (с появлением окостенения апофизов) формируются все типичные признаки заболевания. Появляется боль в спине, особенно при длительной ходьбе и сидении, возникает быстрая утомляемость и слабость мышц спины. Происходит увеличение грудного кифоза. Его образование сопровождается усилением лордоза в шейном и поясничном отделах, одновременно может сформироваться и сколиоз. Деформация приобретает фиксированный характер. Присоединение корешкового синдрома дискогенного происхождения приводит к еще большему ограничению подвижности позвоночника.
В III стадии процесса, соответствующей полному слиянию апофизов с телами позвонков, кифоз и клиновидная деформация тел позвонков несколько уменьшаются. Однако фиксированный кифоз и увеличенный поясничный лордоз остаются в течение всей жизни. Со временем развиваются явления остеохондроза позвоночника с нарастающим болевым синдромом.
Рентгенологически изменения, характерные для остеохондропатии, определяются во II стадии заболевания. Выявляются зазубренность апофизов, клиновидная деформация тел позвонков с увеличением их переднезаднего размера, сужение межпозвонковых дисков, нарушение целостности замыкательных костных пластинок позвонков с образованием грыж Шморля. Формируется патологический кифоз грудного отдела позвоночника (См. рис.).
Лечение. Рекомендуют общеукрепляющее лечение, витаминотерапию, рациональный режим труда и отдыха (спать на жестком), выработку правильной осанки, разгрузку позвоночника. С целью укрепления мышечного корсета назначают лечебную гимнастику, плавание в бассейне, массаж мышц спины. В тяжелых случаях возможно рекомендовать ношение корректора осанки. При рано начатом лечении удается приостановить развитие процесса и образование значительной деформации. В единичных случаях при выраженном кифозе с неврологическими проявлениями показано оперативное лечение.
Остеохондропатия тела позвонка
(Болезнь Кальке, плоский позвонок)
Заболевание впервые описано Кальве в 1925 г. Встречается редко, в основном у мальчиков в возрасте 7-14 лет. В основе патологии лежит асептический некроз губчатого вещества тела позвонка. Длительность заболевания от 2 до 5-6 лет.
Клиника. Проявляется чувством усталости в спине, болью в позвоночнике, болезненностью при надавливании на выступающий остистый отросток больного позвонка. Наклон кпереди и разгибание позвоночника могут быть ограниченными, возможны корешковые симптомы. У большинства детей общее самочувствие хорошее, температура тела нормальная, однако, в отдельных случаях заболевание начинается с подъема температуры до 39,0°С, повышения СОЭ, иногда выявляется эозинофилия.
На рентгенограмме в профильной проекции пораженный позвонок уплотнен, равномерно сплющен и расширен в переднезаднем направлении (платибрахиспондилия). Тело позвонка приобретает вид узкой полоски, передний край его выступает кпереди, межпозвонковые щели расширены.
Лечение. Основа лечения - разгрузка позвоночного столба (постельный режим на спине на жесткой постели или в гипсовой кроватке с реклинирующим валиком под пораженным позвонком), лечебная гимнастика. Лежа проводят массаж, общую и лечебную гимнастику, направленную на реклинацию уплощенного позвонка и укрепление мышц спины (создание мышечного корсета). В стадии восстановления рекомендуют ношение съемного ортопедического корсета, разгружающего позвоночный столб. Отдельные авторы считают целесообразным выполнение заднего спондилодеза с целью стабилизации позвоночника и быстрейшей вертикализации (подъема в вертикальное положение) пациента.
Остеохондропатия головок П-Ш плюсневых костей (болезнь Келера II) Остеохондропатия головки II плюсневой кости встречается преимущественно у девочек в возрасте 10-20 лет. Локализуется в эпифизе головки II, реже Ш, плюсневой кости. В единичных случаях возможно вовлечение в патологический процесс IV и V, а также одновременное поражение II и III плюсневых костей.
Причинами патологии считают хроническую микротравму, статические перегрузки переднего отдела стопы при плоскостопии или вследствие ношения обуви на высоком каблуке. Длительность течения процесса 2-2,5 года, развитие болезни постепенное.
Клиника. Отмечается боль в области головки соответствующей плюсневой кости, усиливающаяся при ходьбе и длительном стоянии. На тыле стопы в области поражения появляется отек без признаков воспаления. Активные и пассивные движения в плюснефапанговом суставе ограничены, может возникнуть укорочение соответствующего пальца. Больные ходят с опорой на пятку, разгружая передний отдел стопы. Боль сохраняется довольно продолжительное время, затем постепенно стихает.
В классическом варианте заболевание проходит стадии, как и при болезни Легга-Кальве-Пертеса
Рентгенологические изменения в 1 стадии могут отсутствовать. Во II стадии головка плюсневой кости теряет свою правильную шаровидную или овоидную форму и уплощается, длина ее уменьшается в 2-3 раза, приводя к укорочению соответствующего пальца. В /// стадии происходит выраженное расширение суставной щели, секвестрация головки с образованием нескольких фрагментов, а в IV- резорбция некро-тизированной кости с ремодуляцией головки, приобретающей блюдцеобразную форму c исходом в деформирующий артроз.
Лечение консервативное. При острых болях и выраженном отеке стопу фиксируют гипсовой лонгетой. После исчезновения острых явлений назначают ортопедическую обувь или стельки-супинаторы, обеспечивающие разгрузку соответствующей головки плюсневой кости. Одновременно проводят электропроцедуры, грязелечение, аппликации парафина и озокерита.
При развитии в области плюснефалангового сустава выраженной деформации с краевыми остеофитами и сильным болевым синдромом – оперативное лечение.
Оетеохондропатия ладьевидной кости стопы
(болезнь Келера I)
Асептический некроз ладьевидной кости стопы встречается преимущественно у мальчиков в возрасте 3-6 лет, но может наблюдаться и в более позднем возрасте (до 12 лет). В качестве этиологических факторов называют травму, а также нарушение развития ладьевидной кости, обусловленное рахитом. Длительность заболевания -1-2 года.
Клиника. Возникают боли, усиливающиеся при ходьбе, и отек тыльной поверхности стопы по ее медиальному краю. Пальпация в проекции ладьевидной кости вызывает выраженную болезненность. С прогрессированием процесса болевой синдром усиливается, при ходьбе опора идет на наружный край стопы, появляется хромота.
На рентгенограмме в начальной стадии выявляется легкий остеопороз, затем уплотнение костной структуры ядра окостенения ладьевидной кости (ядер окостенения может быть два). Появляется сплющивание и фрагментация ладьевидной кости, ее деформация в виде чечевицы или полумесяца. Прилежащие суставные щели расширяются.
Лечение консервативное: разгрузка и иммобилизация конечности гипсовой повязкой с моделированием продольного свода стопы до 1-1,5 мес, затем ограничение статических нагрузок, тепловые процедуры, массаж, электрофорез иодида калия и новокаина, ношение стелек-супинаторов.
Рассекающий остеохондрит - (болезнь Кёнига)
Рассекающие остеохондриты суставных поверхностей - это остеохондропатии с единым этиопатогенезом и различной анатомической локализацией. В основе заболевания лежит нарушение кровообращения в ограниченном участке эпифиза. В результате формируется краевой асептический некроз небольшого участка субхондрально расположенной губчатой кости, форма которого напоминает чечевицу, двояковыпуклую или плосковыпуклую линзу. В дальнейшем происходит полное отделение этого костного фрагмента, покрытого гиалиновым хрящом, в полость сустава и превращение его в «суставную мышь», блокирующую движения в суставе.
Встречается в возрасте 11-60 лет, однако, преимущественно наблюдается у молодых мужчин от 20 до 40 лет. В 90-93% случаев заболевание поражает коленный сустав, в основном внутренний мыщелок бедра. Этиология заболевания окончательно не выяснена. Наибольшее признание получила сосудистая теория, согласно которой аваскулярный некроз возникает вследствие рефлекторного спазма или эмболии конечных сосудов, питающих ограниченный участок эпифиза.
Клиника. В развитии патологического процесса выделяют 3 стадии.
/ стадия заболевания бедна симптомами: боль в коленном суставе разной интенсивности, носит неопределенный характер, возможны явления умеренного синовита.
// стадия. Б боль принимает более постоянный характер, усиливается при ходьбе. Больные испытывают чувство ограничения движений в суставе, снижается опорная функция конечности, может появиться 0щадящая хромота.
III стадия наступае после отделения в полость сустава некротизировавшегося костно-хрящевого фрагмента. Иногда удается прощупать свободно перемещающееся внутрисуставное тело. Величина его может быть от крупной чечевицы до фасоли средних размеров. При ущемлении «суставной мыши» между суставными поверхностями возникает резкая боль и внезапное ограничение движений - блокада сустава. Со временем развивается гипотрофия четырехглавой мышцы бедра и возникают явления артроза.
Рентгенологически в / стадии в субхондральной зоне выпуклой суставной поверхности мыщелка бедра выявляется ограниченный участок уплотнения кости. Обычно он двояковыпуклый, достигает размеров 1,0x1,5 см и ограничен узким ободком просветления. Затем (во II стадии) происходит отграничение уплотненного костно-хрящевого фрагмента от материнского ложа: расширяется зона просветления вокруг него, фрагмент начинает выступать в полость сустава. В /// стадии определяется ниша в области суставной поверхности мыщелка бедренной кости, а внутрисуставное тело обнаруживается в любой части коленного сустава (обычно, в одном из заворотов, а при блокаде сустава - между суставными поверхностями).
Лечение рассекающего остеохондрита зависит от стадии заболевания.
При I и II стадии показано консервативное лечение, включающее ограничение нагрузки с полным исключением прыжков и бега, иммобилизацию больной конечности гипсовой шиной, физиотерапевтические процедуры (фонофорез хондроксида или гидрокортизона, электрофорез хлорида кальция, парафино-озокеритовые аппликации), применение хондропротекторов (мукосата, структума).
Оперативное лечение показано в Ш стадии заболевания (при наличии свободного костно-хрящевого фрагмента, блокирующего сустав и поддерживающего явления хронического синовита), а также является методом выбора при II стадии патологических изменений.
Остеохондропатия полулунной кости кисти
(болезнь Кинбека)
Заболевание впервые описано австрийским рентгенологом Кинбеком (1910). В основе патологии лежит субхондральный некроз полулунной кости запястья. Наблюдается преимущественно у лиц мужского пола в возрасте от 17 до 40 лет, подверженных частым повторным травмам кисти. Играет значение и постоянное перенапряжение кисти в процессе интенсивного ручного труда у слесарей, токарей, плотников, столяров. Процесс чаше локализуется на правой руке.
Клиника. Отмечается локальная боль и припухлость в области полулунной кости. При движениях и пальпации болевые ощущения усиливаются, особенно при разгибании кисти, сжатой в кулак. Постепенно нарастает ограничение подвижности в лучезапястном суставе, больше страдает тыльная флексия кисти. Сила сжатия пальцев в кулак значительно снижена, развивается гипо трофия мышц предплечья. Исход заболевания - артроз суставов запястья, обусловленный возникновением в них подвывихов из-за уменьшения в объеме полулунной кости.
При рентгенологическом исследовании в ранней стадии заболевания отмечается смазанная картина структурного рисунка полулунной кости. Со временем тень ее становится более интенсивной по сравнению с соседними костями запястья, размеры уменьшаются, появляется неровность контуров, могут возникать кистозные изменения. В дальнейшем развивается фрагментация, сплющивание прогрессирующая деформация полулунной кости, которая часто приобретает треугольную форму (См. рис.). Смежные суставные щели при этом расширяются. Иногда происходит уменьшение размеров полулунной кости с явлениями повышенного склероза костной ткани, напоминающего мраморную болезнь. В позднем периоде заболевания рентгенологически определяются явления артроза.
Лечение. В начальных стадиях применяют консервативное лечение: фиксацию лучезапястного сустава гипсовой шиной в положении легкой тыльной флексии, тепловые процедуры, ультразвук, магнито- и лазеротерапию. При ранней диагностике и длительном лечении консервативная терапия дает определенный положительный эффект.
Существует более 20 способов оперативного лечения болезни Кинбека. В начальных стадиях заболевания для уменьшения сплющивания полулунной кости применяют метод лигаментотензии (растяжения) в аппарате Илизарова. При развитии выраженной деформации для улучшения функции кистевого сустава делают частичные артродезы. При субтотальном и тотальном поражении прибегают к полному удалению некротизированной полулунной кости.
Остеохондропатия бугра пяточной кости
(болезнь Халгунда-Шинца)
Остеохондропатия апофиза пяточной встречается чаще у девочек в возрасте 12-16 лет. Причина возникновения - частая травма пяток и перенапряжение ахиллова сухожилия и сухожилий подошвенных мышц при занятиях спортом.
Клиника. Заболевание начинается с острых или постепенно нарастающих болей в области бугра пяточной кости, возникающих после нагрузки. При пальпации или разгибании стопы болевой синдром усиливается. Над пяточным бугром, у места прикрепления ахиллова сухожилия, отмечается припухлость. Пациенты ходят с опорой на передний отдел стопы; бег, прыжки, занятия спортом становятся невозможными.
На рентгенограммах в боковой проекции, определяется уплотнение апофиза, расширение щели между апофизом и пяточной костью. Трудности рентгенологической диагностики связаны с тем, что в норме апофиз пяточной кости у детей имеет до 4-х ядер окостенения, среднее из которых, как правило, уплотнено, а смежные поверхности пяточной кости и апофиза зазубрены.
Наиболее характерным рентгенологическим признаком остеохондропатии является пятнистая структура уплотненного ядра окостенения. В дальнейшем наступает фрагментация апофиза, а затем и его перестройка - формируется новое губчатое вещество кости.
Лечение консервативное. Ограничивают физическую нагрузку, на время лечения прекращают занятия спортом. Применяют теплые ванночки и физиотерапевтическое лечение: электрофорез новокаина, ультразвук, диатермию. При сильном болевом синдроме назначают постельный режим, накладывают гипсовую повязку с моделированием сводов стопы. После ликвидации болей разрешают нагрузку на конечность в обуви с широким устойчивым каблуком. Для ослабления нагрузки на пяточную кость рекомендуют ношение ортопедических стелек-супинаторов с выкладкой сводов стопы. В отдельных случаях применяют туннелизацию бугра пяточной кости по Беку.
